- 首页
- >>
- 资源中心
- >>
- 技术资源
- >>
- 病毒载体与细胞技术平台
- >
- 文章详情
稳定细胞系构建方法解析
- 2026-03-19
- 5
在生物医学研究领域,构建稳定细胞系是基因功能研究和重组蛋白表达的核心技术,稳定细胞系与瞬时转染不同,它能够长时间持续表达外源基因,可为科学研究提供稳定的实验模型。
一、技术流程与方法选择
构建稳定细胞系的第一步是选择合适的亲本细胞,常用的细胞系包括HEK293、CHO、HeLa等,这些细胞生长稳定、易于转染。挑选细胞系时,需结合其遗传背景、生长特性及与研究目的的匹配度来综合考虑,这是成功获得定制细胞系的基础。
载体设计是决定构建成功的关键因素。一个完整的表达载体应包含以下元件:
强效启动子(如CMV、EF1α)
多克隆酶切位点
筛选标记基因(如嘌呤霉素、新霉素抗性基因)
增强子元件和polyA信号
选择转染方式时,科研人员要依据细胞种类与实验要求选定最优方案:化学转染中的脂质体法操作简单适用于多数贴壁细胞;物理转染如电穿孔对悬浮细胞效果明显病毒转染法效率最高需要更高的生物安全防护级别。
二、筛选流程与单克隆化
转染后的筛选工作需系统调整。第一步用杀灭曲线实验确定最佳抗生素浓度,该环节对构建稳定细胞系很关键,筛选时间一般2-4周,此阶段要定期更换筛选培养基,逐步清除未转染成功的细胞。
单克隆化是获得纯系细胞的关键步骤。目前主要采用的方法包括:
有限稀释法:最经典的单克隆分离技术
克隆环法:适用于贴壁性强的细胞
流式细胞分选:效率最高但需要特殊设备
半固体培养基法:可实时观察克隆形成过程
在筛选过程中,用报告基因系统可大幅提升筛选成效。绿色荧光蛋白(GFP)及其变体能直观呈现转染效率,荧光素酶报告系统可定量衡量基因表达水平,这类系统在打造定制细胞系过程中作用特别关键。
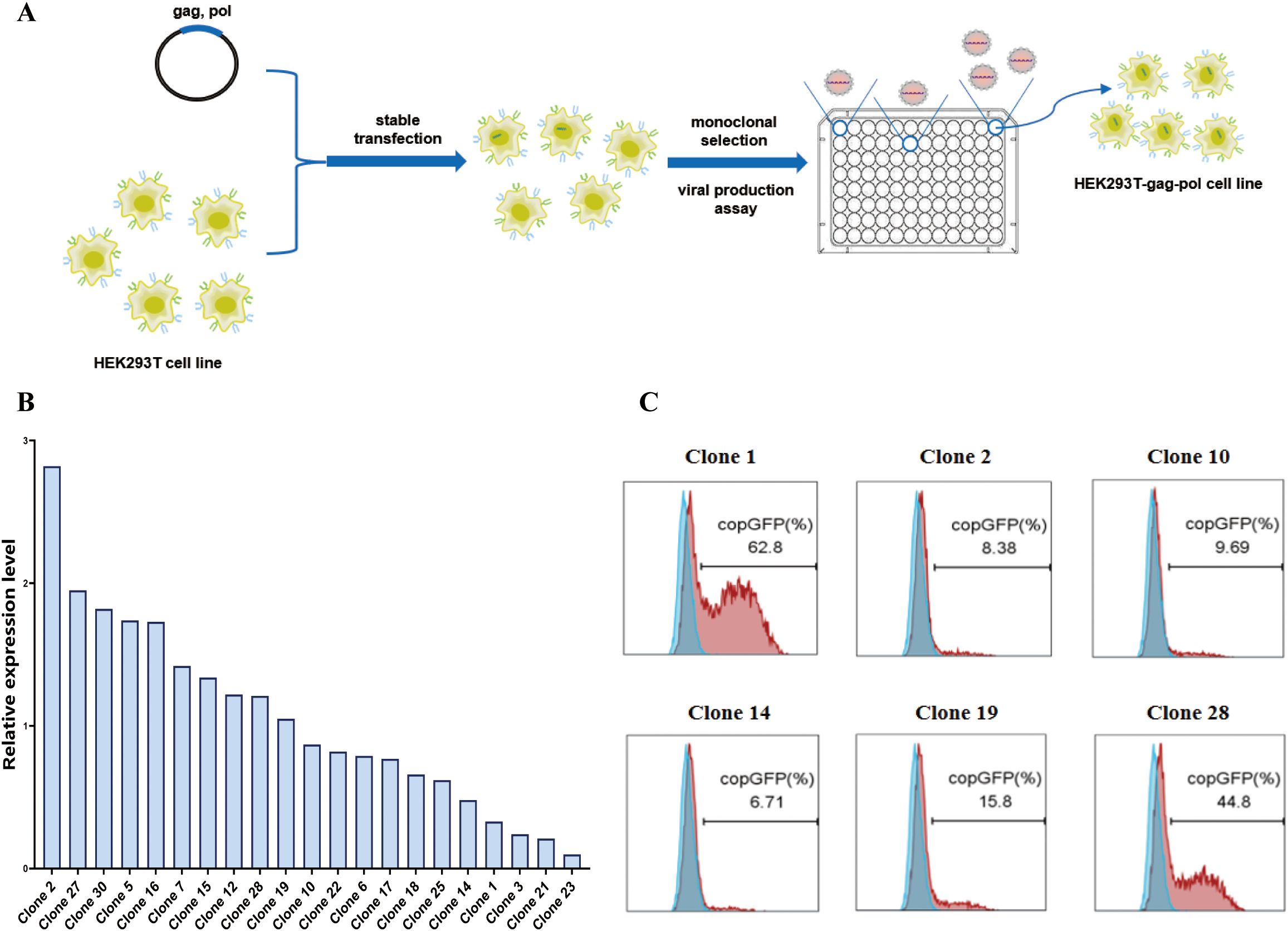
图1 HEK293T-gag-pol细胞系的构建
三、验证方法与质量控制
获得单克隆细胞后,需要进行多层次的验证。基因组水平的验证包括:
1. PCR检测外源基因整合
2. Southern blot分析拷贝数
3. 测序确认基因序列完整性
转录层面验证主要用RT-qPCR技术检测基因表达量,还可以采用Northern blot技术做补充验证。蛋白层面检测手段包含Western blot、免疫荧光染色及流式细胞术等,这类技术可直接确认目标蛋白的表达情况与定位信息。
在建立稳定细胞系的过程中,质量控制尤为重要。需要定期检测以下指标:
细胞遗传稳定性
外源基因表达持续性
微生物污染情况
细胞形态和生长特性
四、技术优化与问题解决
在实际操作中,常会遇到转染效率低、基因沉默等问题,可采取以下优化措施:
1. 提高转染效率的方法:
优化DNA与转染试剂比例
调整细胞接种密度
改进培养基成分
采用不同转染方法组合
2. 防止基因沉默的策略:
使用基质附着区元件
选择去甲基化试剂处理
采用不同启动子组合
定期进行压力筛选
3. 对于表达量不稳定的问题,可以考虑以下解决方案:
增加基因拷贝数
使用更强大的启动子
优化培养条件和时间
采用诱导表达系统
五、特殊技术与创新方法
基因编辑技术的发展为构建稳定细胞系带来全新工具。CRISPR/Cas9系统可精准整合基因,显著提升同源重组效率。该方法尤其适用于打造基因敲入或点突变的定制细胞系。
诱导表达系统运用让基因表达调控更为精准。四环素诱导系统借助添加或去除doxycycline能达成基因表达的时空调控,这在研究毒性基因或重要功能基因时具备独特优势。
无标记筛选技术研发攻克了筛选标记会干扰细胞生理状态的难题。Cre-loxP系统与FLP-FRT系统可完成筛选标记的精准移除,获得更贴近天然状态的稳定细胞系。
位点特异性整合技术的运用大幅提升了表达一致性。借助把外源基因定点整合至基因组的高表达位点可有效规避位置效应,得到表达水平更均一的细胞群体。
依靠这些系统化方法与技术创新研究人员可更高效构建契合实验需求的稳定细胞系,各个技术环节的优化或许大幅提升构建成功率,实验设计中需综合考量各类因素挑选最适配的技术路线。卡梅德生物在稳定细胞系构建以及原代细胞定制等方面有着丰富的经验,可为客户提供一站式服务,欢迎前来咨询!
[1] Wurm FM. Production of recombinant protein therapeutics in cultivated mammalian cells. Nat Biotechnol. 2004 Nov;22(11):1393-8.
[2] Urlaub G, Chasin LA. Isolation of Chinese hamster cell mutants deficient in dihydrofolate reductase activity. Proc Natl Acad Sci U S A. 1980 Jul;77(7):4216-20.
[3] Li J, Menzel C, Meier D, Zhang C, Dübel S, Jostock T. A comparative study of different vector designs for the mammalian expression of recombinant IgG antibodies. J Immunol Methods. 2007 Jan 10;318(1-2):113-24.
[4] Chavez M, Rane DA, Chen X, Qi LS. Stable expression of large transgenes via the knock-in of an integrase-deficient lentivirus. Nat Biomed Eng. 2023 May;7(5):661-671.
[5] Bai F, Cai P, Yao L, Shen Y, Li Y, Zhou YJ. Inducible regulating homologous recombination enables precise genome editing in Pichia pastoris without perturbing cellular fitness. Trends Biotechnol. 2025 Jun;43(6):1385-1402.
[6] Zhao L, Qiu C, Chen H, Yu Z, Fan J, Ma Q, Zhan S, Feng Y, Li X, Ma P, Wang W, Shi Y, Xu JF, Wang J. Construction of stable packaging cell lines for large-scale industrial BaEV-enveloped retroviral vector production. Front Immunol. 2025 May 26;16:1578660
- 构建稳定细胞系
- 稳定细胞系
- 细胞系构建
- 定制细胞系
-
 400-621-6806
400-621-6806 -
 13116038708(微信同号)
13116038708(微信同号) -
 周一至周五 8:30-18:00
周一至周五 8:30-18:00 -

-
 0
0
-





