纳米抗体:解锁脑部疾病治疗的新一代生物药利器
- 2025-11-26
- 273
在神经科学与药物研发领域中,让治疗分子高效进入大脑内部是攻克脑部相关病症的关键挑战之一。传统抗体类药物分子尺寸偏大,难以穿透血脑屏障,导致在脑部的抗体应用范围有局限性。而骆驼科动物来源的纳米抗体凭借自身独特优势破解这一难题,为脑部疾病治疗带来突破性全新契机。
本文参考《Trends in Pharmacological Sciences》发表的权威综述,深入剖析这一新兴技术平台的巨大发展潜力。
一、 什么是纳米抗体?为何它们独具优势?
● 起源与结构:纳米抗体也称为VHH抗体,是骆驼科动物(包括羊驼、骆驼)体内天然存在的重链抗体可变区片段。不同于由两条重链和两条轻链组成的传统IgG抗体,VHH抗体仅由重链可变区构成,是具备功能的最小抗原结合片段。
● 特性:纳米抗体的分子量约15 kDa,大小仅为传统抗体的十分之一,但比常规的小分子药物大,其独特尺寸使其兼具抗体药物与小分子药物的优势:
1. 高亲和力与高特异性:与传统抗体一样,纳米抗体通过其互补决定区精确识别靶点,确保精准打击。
2. 出色的组织穿透性:小尺寸使其更容易穿透致密组织,包括血脑屏障。
3. 高溶解性与稳定性:不同于许多疏水的小分子,纳米抗体水溶性好,降低了脱靶风险。
4. 可触及隐秘表位:其长CDR3环能够结合传统抗体难以触及的蛋白隐藏表位或构象表位,从而精确调控受体功能。
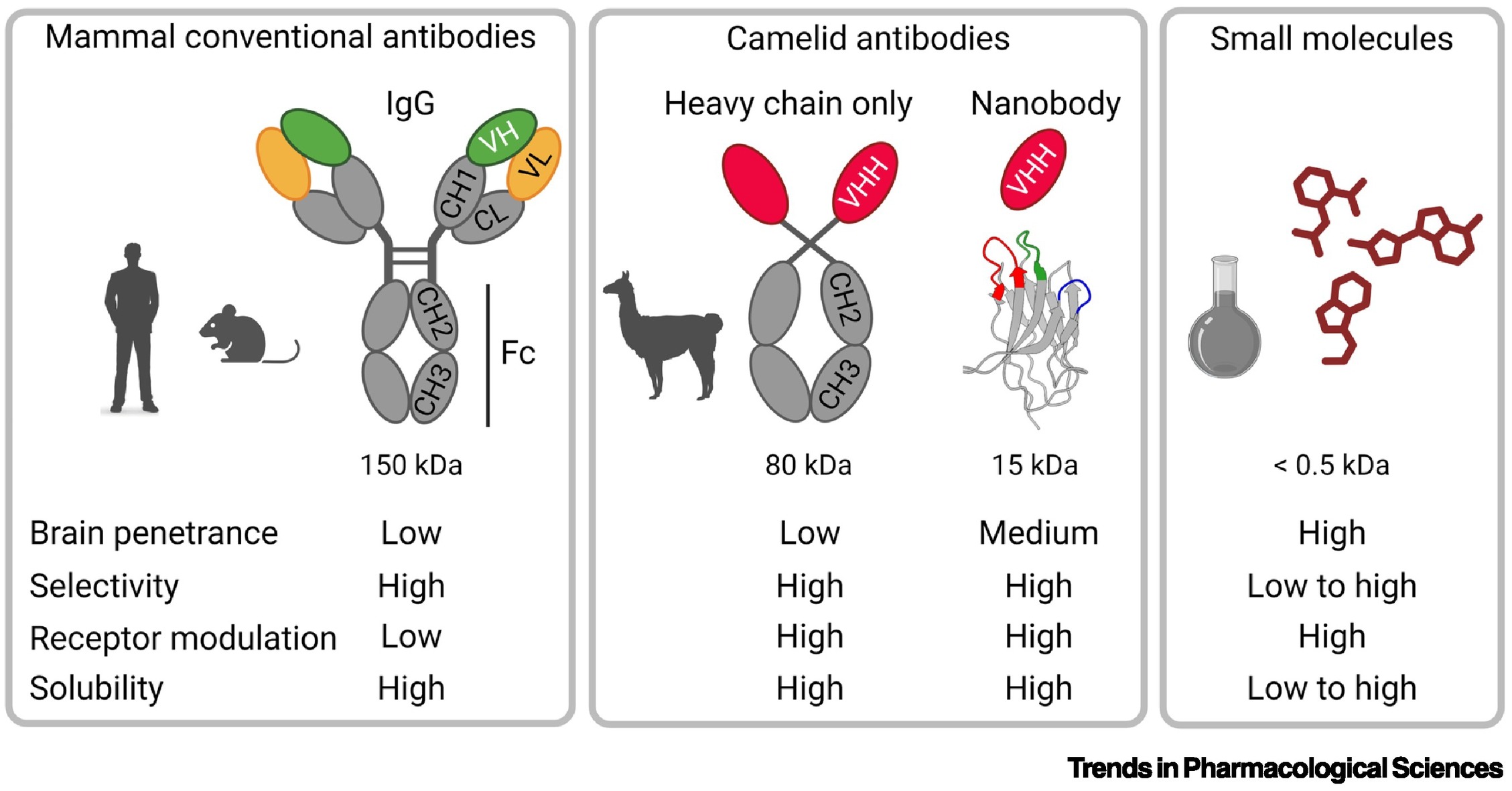
纳米抗体在尺寸、选择性、溶解性和受体调控能力方面取得了最佳平衡,是中枢神经系统靶向药理学的理想工具。
二、纳米抗体成功治疗脑部疾病的实证
尽管纳米抗体在药理上优势突出,但学界长期存在固有认知便是:纳米抗体体积小巧,易在血液中被肾脏迅速清除,难以顺利抵达大脑。而最新研究已有力颠覆这一认知。
◆ 阿尔茨海默病抗体应用探索:研究显示,多个科研团队已开发靶向Aβ及tau蛋白的纳米抗体:靶向Aβ的纳米抗体在实验模型中表现出良好脑内穿透效果及淀粉样斑块识别能力;靶向tau的纳米抗体在神经元层面可有效阻止tau蛋白摄取,遏制其神经毒性扩散蔓延。
◆ 精神分裂症治疗的标志性进展:研究人员研发出的双价纳米抗体可作为代谢型谷氨酸受体mGlu2的正构变构调节剂,这种纳米抗体经腹腔注射后,可成功穿透血脑屏障,并在与认知功能相关的皮层及海马区聚集,最终在两个模拟精神分裂症的小鼠模型中大幅恢复了动物的认知。
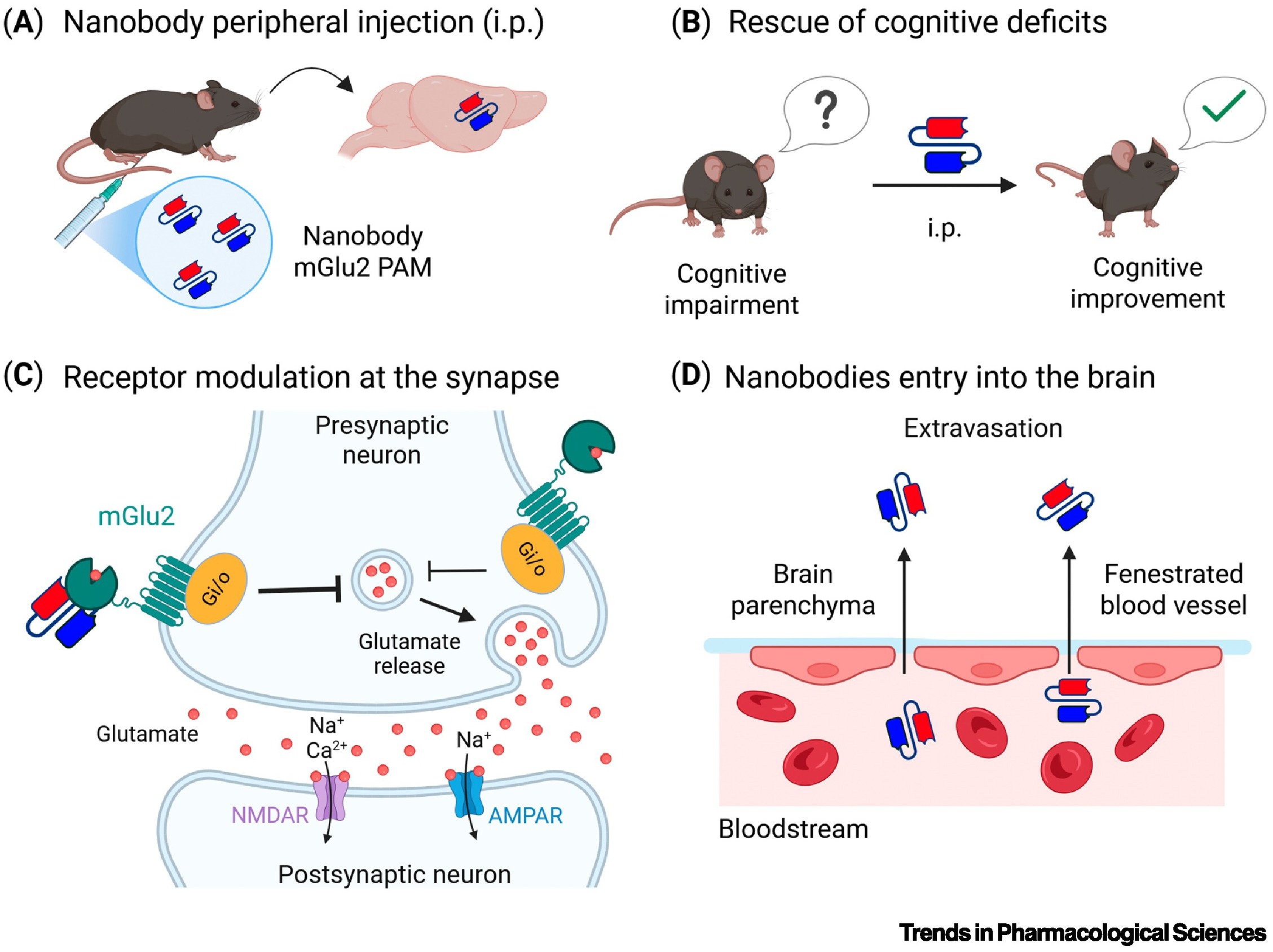
图2 一种针对谷氨酸受体的纳米抗体可挽救 N-甲基-D-天冬氨酸(NMDA)功能减退型精神分裂症小鼠模型的认知缺陷
三、纳米抗体进入大脑的多种可能路径
那么,纳米抗体究竟是如何突破血脑屏障这一坚固防线的呢?其机制多样,为我们的抗体应用设计提供了多种思路:
1. 通过多孔血管直接外渗:初步证据表明,纳米抗体可通过脑部某些区域的“有窗”血管直接外渗进入脑实质。这条路径对IgG等大于60 kDa的蛋白质是关闭的,但纳米抗体却能利用此通道。
2. 受体介导的穿胞作用:这是一种主动运输策略。对VHH抗体进行工程化改造,使其同时靶向血脑屏障上高表达的转运受体(如转铁蛋白受体),从而被带入进大脑。
3. 吸附介导的穿胞作用:通过调整纳米抗体的表面电荷,使其与带负电的血管内皮细胞膜发生静电相互作用,从而被细胞摄取并转运。
4. 病理条件下的被动扩散:在神经炎症或脑肿瘤等疾病状态下,BBB完整性被破坏,纳米抗体可借此机会被动扩散入脑。
5. 替代递送策略:除了直接注射蛋白质,还可以通过腺相关病毒载体在脑细胞内直接表达纳米抗体,或通过鼻内给药利用嗅觉通路直接入脑。
VHH抗体凭借其单域结构与独特折叠特性,在多种表达系统中均能高效形成天然构象,可以根据不同人群的不同需求进行低成本、大规模的生产,如今已逐步成为脑部疾病诊疗领域极具潜力的新方向,为脑类疾病的治疗带来了全新的希望。
卡梅德生物的核心服务覆盖从早期的纳米抗体筛选与定制、抗体人源化,到后期的稳定细胞系构建等关键环节,为科研工作者提供高效全流程研发助力。
参考文献
[1] Lafon PA, Prézeau L, Pin JP, Rondard P. Nanobodies: a new paradigm for brain disorder therapies. Trends Pharmacol Sci. 2025 Nov;46(11):1049-1051.
[2] Oosterlaken M, Rogliardo A, Lipina T, et al. Nanobody therapy rescues behavioural deficits of NMDA receptor hypofunction. Nature. 2025 Sep;645(8079):262-270.
常见问题解答
Q1:纳米抗体作为外来蛋白质,其免疫原性如何?在临床治疗中如何应对这一问题?
A1:尽管纳米抗体源自骆驼科动物,其氨基酸序列与人类存在差异,因此在人体内确实存在引发免疫反应的风险,可能导致产生抗药物抗体,影响疗效和安全性。这是其临床转化中必须谨慎评估的关键问题。
为应对这一挑战,科研与产业界已发展出多重有效策略:
(1)人源化改造:这是最核心的手段。通过分子生物学技术,将纳米抗体框架区中非关键的、可能被人体免疫系统识别为“异己”的氨基酸残基,替换为人类抗体中常见的相应残基。这能显著降低其免疫原性,同时尽可能保留其高亲和力和稳定性。
(2)生成完全人源的纳米抗体:虽然技术挑战更大,但研究者正尝试从人源天然单域抗体库中筛选VH片段,或利用转基因小鼠平台生成完全人源的类似物,以期从源头上解决免疫排斥问题。
(3)全面的临床评估:在药物开发过程中,会通过体外免疫原性预测模型和体内实验进行早期风险评估。在临床试验阶段,则会严密监测患者体内抗药物抗体的产生情况及其对药代动力学、药效学和安全性的实际影响。
Q2:纳米抗体在生产制造上与传统抗体相比有何优势?
A2:纳米抗体的生产兼具了部分小分子和抗体的特性,形成了独特且更具成本效益的制造路径。其核心优势在于卓越的可表达性和稳定性。
由于其结构简单、不含复杂的链间二硫键和糖基化修饰,纳米抗体可以在成本低廉的大肠杆菌或酵母等微生物系统中进行高效、高产量地表达。这彻底避免了传统抗体必须使用哺乳动物细胞(如CHO细胞)的复杂、昂贵且耗时的生产过程。此外,它们卓越的物理化学稳定性使其在发酵、纯化和储存过程中更不易降解和聚集,从而提高了最终产品的得率和均一性。
当然,挑战也同样存在,例如因其分子量小,在采用常规层析纯化时需要更精细的工艺控制。但总体而言,纳米抗体在规模化生产上具有显著的成本和效率优势,更易于实现大规模、低成本的生产,这对降低未来药物的价格至关重要。
Q3:除了已提到的疾病,纳米抗体在哪些其他脑部疾病中有应用潜力?
A3:纳米抗体平台的灵活性使其在多种中枢神经系统疾病中具有广阔的应用前景,远超阿尔茨海默病和精神分裂症。
(1)在帕金森病领域,可以设计靶向α-突触核蛋白聚集体的纳米抗体,用以抑制其病理性纤维的形成和细胞间传播。
(2)对于脑肿瘤,纳米抗体可作为“特洛伊木马”,通过靶向血脑屏障上的受体主动进入大脑,并进一步与靶向肿瘤特异性抗原的纳米抗体组成双特异性药物,将抗癌效应精准递送至胶质母细胞瘤等肿瘤内部。
(3)在疼痛管理领域,可以开发靶向疼痛通路中关键受体(如特定亚型的阿片受体)的纳米抗体,通过变构调节等方式实现精准镇痛,同时有望避免成瘾等副作用。这些探索性研究正在蓬勃发展,预示着纳米抗体有望成为中枢神经系统药物开发的通用型强大工具。
Q4:什么是噬菌体展示技术?它在纳米抗体制备中为何如此重要?
A4:噬菌体展示是纳米抗体筛选最核心、最成熟的技术平台。其原理是将编码数十亿种不同纳米抗体的基因片段,与编码噬菌体(一种病毒)外壳蛋白的基因融合,使得每一个噬菌体颗粒表面都能“展示”一种独特的纳米抗体,而其内部则包含着该纳米抗体的基因。
这个过程如同制作一个分子级别的“身份证”库。当我们需要寻找能结合特定靶点(如新冠病毒的S蛋白)的纳米抗体时,只需让这个庞大的噬菌体库与固定的靶点接触。那些无法结合的噬菌体会被洗掉,而能够特异性结合的极少数“精英”则被保留下来。这些被筛选出的噬菌体经过感染细菌进行扩增后,可以开始下一轮更严格的筛选。通常经过3-5轮的“吸附-洗涤-洗脱-扩增”循环,与靶点亲和力最高、特异性最强的纳米抗体就会被富集出来。最后,通过测序展示该纳米抗体的噬菌体基因,就能获得其精确的氨基酸序列,用于后续生产。
Q5:获得纳米抗体序列后,如何大规模生产?主要挑战是什么?
A5:一旦通过筛选获得理想纳米抗体的基因序列,大规模生产通常使用微生物发酵系统,尤其是大肠杆菌。
其标准流程是:将纳米抗体基因克隆到表达载体中,然后转入经过优化的大肠杆菌工程菌株。在可控的发酵罐中,通过诱导剂(如IPTG)启动基因表达,菌体便会大量合成纳米抗体。随后,通过破碎菌体、收集上清或包涵体,再经过一系列层析纯化步骤(如亲和层析、离子交换层析等),即可获得高纯度的纳米抗体产品。
-
 400-621-6806
400-621-6806 -
 13116038708(微信同号)
13116038708(微信同号) -
 周一至周五 8:30-18:00
周一至周五 8:30-18:00 -

-
 0
0
-





