纳米抗体:解锁脑部疾病治疗的新一代生物药利器!
- 2026-04-29
- 5
发表在《Trends in Pharmacological Sciences》,IF=19.9,题目为《Nanobodies: a new paradigm for brain disorder therapies》的研究综述中指出在神经科学与药物研发领域中,让治疗分子高效进入大脑内部是攻克脑部相关病症的关键挑战之一。传统抗体类药物分子尺寸偏大,难以穿透血脑屏障,导致在脑部的抗体应用范围有局限性。而骆驼科动物来源的纳米抗体凭借自身独特优势破解这一难题,为脑部疾病治疗带来突破性全新契机,本篇综述将深入剖析这一新兴技术平台的巨大发展潜力。
一、 什么是纳米抗体?为何它们独具优势?
起源与结构:纳米抗体也称为VHH抗体,是骆驼科动物(包括羊驼、骆驼)体内天然存在的重链抗体可变区片段。不同于由两条重链和两条轻链组成的传统IgG抗体,VHH抗体仅由重链可变区构成,是具备功能的最小抗原结合片段。
特性:纳米抗体的分子量约15 kDa,大小仅为传统抗体的十分之一,但比常规的小分子药物大,其独特尺寸使其兼具抗体药物与小分子药物的优势:
高亲和力与高特异性:与传统抗体一样,纳米抗体通过其互补决定区精确识别靶点,确保精准打击。
出色的组织穿透性:小尺寸使其更容易穿透致密组织,包括血脑屏障。
高溶解性与稳定性:不同于许多疏水的小分子,纳米抗体水溶性好,降低了脱靶风险。
可触及隐秘表位:其长CDR3环能够结合传统抗体难以触及的蛋白隐藏表位或构象表位,从而精确调控受体功能。
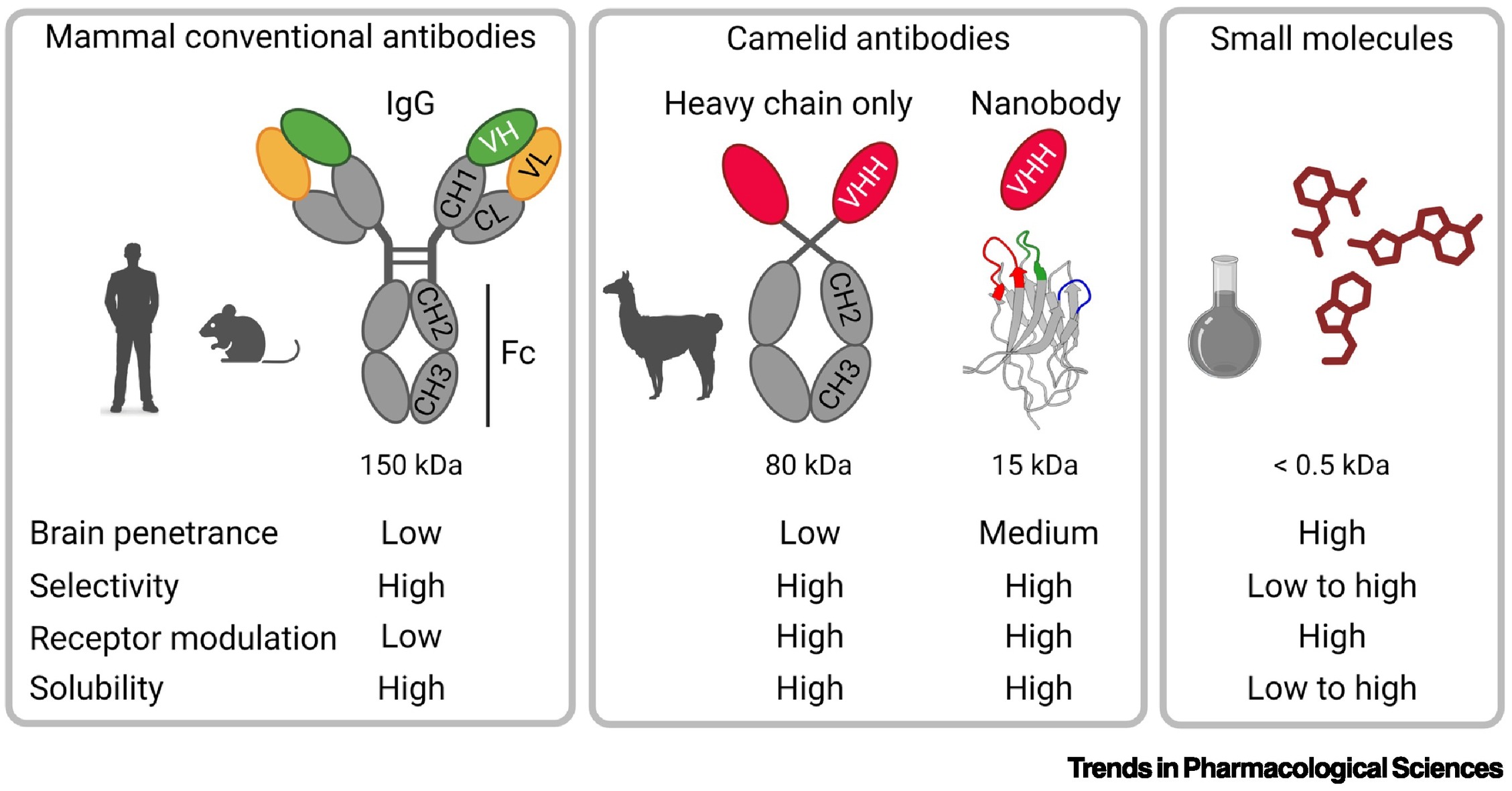
图1 纳米体在中枢神经系统靶向药理学方面具有独特的特点
纳米抗体在尺寸、选择性、溶解性和受体调控能力方面取得了最佳平衡,是中枢神经系统靶向药理学的理想工具。
二、纳米抗体成功治疗脑部疾病的实证
尽管纳米抗体在药理上优势突出,但学界长期存在固有认知便是:纳米抗体体积小巧,易在血液中被肾脏迅速清除,难以顺利抵达大脑。而最新研究已有力颠覆这一认知。
阿尔茨海默病抗体应用探索:研究显示,多个科研团队已开发靶向Aβ及tau蛋白的纳米抗体:靶向Aβ的纳米抗体在实验模型中表现出良好脑内穿透效果及淀粉样斑块识别能力;靶向tau的纳米抗体在神经元层面可有效阻止tau蛋白摄取,遏制其神经毒性扩散蔓延。
精神分裂症治疗的标志性进展:研究人员研发出的双价纳米抗体可作为代谢型谷氨酸受体mGlu2的正构变构调节剂,这种纳米抗体经腹腔注射后,可成功穿透血脑屏障,并在与认知功能相关的皮层及海马区聚集,最终在两个模拟精神分裂症的小鼠模型中大幅恢复了动物的认知。
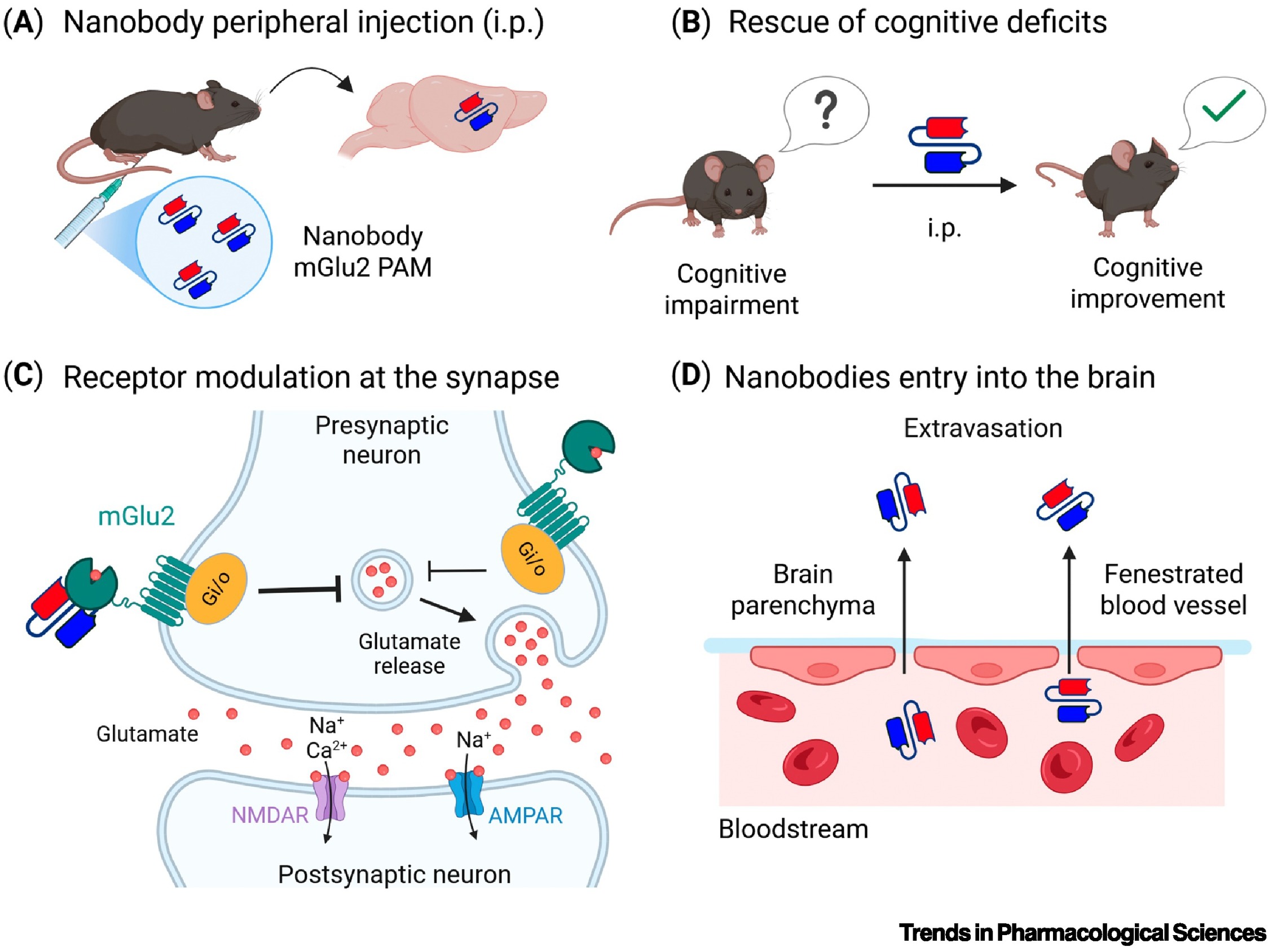
图2 一种针对谷氨酸受体的纳米抗体可挽救 N-甲基-D-天冬氨酸(NMDA)功能减退型精神分裂症小鼠模型的认知缺陷
三、纳米抗体进入大脑的多种可能路径
那么,纳米抗体究竟是如何突破血脑屏障这一坚固防线的呢?其机制多样,为我们的抗体应用设计提供了多种思路:
通过多孔血管直接外渗:初步证据表明,纳米抗体可通过脑部某些区域的“有窗”血管直接外渗进入脑实质。这条路径对IgG等大于60 kDa的蛋白质是关闭的,但纳米抗体却能利用此通道。
受体介导的穿胞作用:这是一种主动运输策略。对VHH抗体进行工程化改造,使其同时靶向血脑屏障上高表达的转运受体(如转铁蛋白受体),从而被带入进大脑。
吸附介导的穿胞作用:通过调整纳米抗体的表面电荷,使其与带负电的血管内皮细胞膜发生静电相互作用,从而被细胞摄取并转运。
病理条件下的被动扩散:在神经炎症或脑肿瘤等疾病状态下,BBB完整性被破坏,纳米抗体可借此机会被动扩散入脑。
替代递送策略:除了直接注射蛋白质,还可以通过腺相关病毒载体在脑细胞内直接表达纳米抗体,或通过鼻内给药利用嗅觉通路直接入脑。
四、总结
VHH抗体凭借其单域结构与独特折叠特性,在多种表达系统中均能高效形成天然构象,可以根据不同人群的不同需求进行低成本、大规模的生产,如今已逐步成为脑部疾病诊疗领域极具潜力的新方向,为脑类疾病的治疗带来了全新的希望。
天津卡梅德生物专注于纳米抗体筛选与开发,提供天然、免疫、合成纳米抗体库构建服务,构建的VHH文库具有出色的多样性和大容量,库容量超过1x 10^9 CFU/mL,能够有效促进客户的研究和项目开发,核心服务覆盖从早期的纳米抗体筛选与定制、抗体人源化,到后期的稳定细胞系构建等关键环节,助力高效抗体发现。
-
 400-621-6806
400-621-6806 -
 614353794
614353794 -
 周一至周五 9:00-18:00
周一至周五 9:00-18:00 -

-
 0
0
-





