纳米抗体的表达纯化与系统选择
- 2025-08-08
- 179
一.纳米抗体的背景
1993年比利时科学家在骆驼外周血中发现一种天然缺失轻链的重链抗体,随着研究的深入,又在鲨鱼等软骨鱼中发现了一种比重链抗体更小的抗体,叫做纳米抗体或单域抗体,纳米抗体是常规抗体的一个重链可变区(VH),由大约120个氨基酸组成,晶体直径为2.5 nm,长度为4 nm,重量仅为12~15 kb,是迄今为止能够结合抗原的最小单位。纳米抗体具有分子量小、亲和力强、组织穿透能力强、抗原识别能力强等优点可以穿透血脑屏障以及实体瘤等组织结合更深层次的抗原表位。纳米抗体可以偶联放射性元素或分子探针用于机体检测成像,基于纳米抗体开发的CAR-T、CAR-NK、TCR-T等免疫细胞疗法以及NDC(纳米抗体欧联药物)的研究层出不穷。
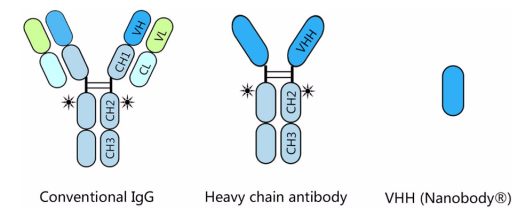
图1.不同种类的抗体
二.重组纳米抗体表达及纯化
通常在纳米抗体的表达上我们会以羊驼外周血中的重链抗体序列为模板扩增其VH区,并将其连接在重组质粒上进行体外重组表达。针对不同的应用场景,所采用的重组抗体的构建方式也是不同的。
VHH抗体表达过程中我们可以应用场景偶联不同的标签蛋白,便于蛋白检测及纯化。例如VHHs融合his tag用于常规的ELISA、Western blot、流式细胞术等;VHHs和IgG的Fc结构域偶联成的重组抗体表现出抑制肿瘤细胞活性的作用,还可能延长VHHs的在机体内的停留时间;VHHs融合AVi-tag生物素化可用于SPR或BLI等检测方法,检测其与靶蛋白的亲和力。针对以上构建策略,我们在纳米抗体表达纯化方面也有不同的方式,His标签融合的VHHs选用Ni柱结合,咪唑盐溶液进行洗脱;Fc标签融合的VHHs选用Protein A/G纯化柱结合,用PH值不同的甘氨酸缓冲液进行洗脱并加入中和缓冲液,使其PH值在7.4左右。
三.纳米抗体表达系统
针对不同的客户需求,卡梅德生物在VHHs抗体表达上会选用合适的表达系统。
1.原核表达系统(大肠杆菌表达系统)
在大肠杆菌中,它们的表达是不稳定的,因为许多VHHs含有一个额外的二硫键,将CDR3与CDR1的末端或CDR2的开头连接起来,在还原细胞质中,VHHs可以以可溶性形式或作为包涵体 (IB) 产生,包涵体可以被重溶解并重新折叠成功能形式但是二硫键是不能形成的,需要氧化环境以形成二硫键的VHHs可以以可溶性和活性形式分泌到氧化周质区室中。在某些情况下,VHHs也可以分泌到培养基中,以便于下游处理。所以对于VHHs的空间结构要求不严格的应用可以采用原核的方式进行表达。
2.哺乳动物表达系统
哺乳动物细胞表达系统是一种最接近人体蛋白翻译后修饰的表达系统,可进行正确的糖基化、磷酸化、羧基化等修饰,其适用于功能性抗体的表达,哺乳动物细胞表达的蛋白通常具有高活性和低免疫原性,符合药物生产要求,其中,CHO细胞和HEK293细胞是最受欢迎的宿主,瞬时转染可用于快速小规模生产VHHs。哺乳动物细胞表达系统除了适用于抗体之外,细胞因子、生长因子、复杂膜蛋白、生物制药和蛋白治疗药物等的制备也同样适用。
昆虫细胞杆状病毒表达系统使用杆状病毒感染昆虫细胞,实现高水平蛋白表达,可进行翻译后修饰,包括糖基化、二硫键、磷酸化等修饰,与哺乳动物细胞表达水平相近。其不足之处在于表达速度较慢,通常需要1-2周才能获得表达蛋白,培养成本也较高,昆虫细胞培养基价格较贵,不及大肠杆菌和酵母经济。该系统还展示了N-聚糖相关的应用微生物生物技术,药物糖蛋白表达问题;然而,通过使用特定的昆虫细胞系或含有甘糖基转移酶的细胞,可以产生哺乳动物类型的N-聚糖。Gómez-Sebastián等人第一次使用改良杆后的状病毒表达系统进行VHHs重组抗体的表达。
引用:
[1] Sun S, Ding Z, Yang X, Zhao X, Zhao M, Gao L, Chen Q, Xie S, Liu A, Yin S, Xu Z, Lu X. Nanobody: A Small Antibody with Big Implications for Tumor Therapeutic Strategy. Int J Nanomedicine. 2021 Mar 22;16:2337-2356.
[2] Verhaar ER, Woodham AW, Ploegh HL. Nanobodies in cancer. Semin Immunol. 2021,52:101425.
[3] Golas MM, Jayaprakash S, Le LTM, Zhao Z, Heras Huertas V, Jensen IS,Yuan J, Sander B. Modulating the Expression Strength of the Baculovirus/Insect Cell Expression System: A Toolbox Applied to the Human Tumor Suppressor SMARCB1/SNF5. Mol Biotechnol. 2018, 60(11):820-832.
[4] Osz-Papai J, Radu L, Abdulrahman W, Kolb-Cheynel I, Troffer-Charlier N, Birck C, Poterszman A. Insect cells-baculovirus system for the production of difficult to express proteins. Methods Mol Biol. 2015, 1258:181-205.
[5] Fu Y, Han Z, Cheng W, Niu S, Wang T, Wang X. Improvement strategies for transient gene expression in mammalian cells. Appl Microbiol Biotechnol. 2024, 108(1):480.
- 纳米抗体
- VHH抗体表达
- 重组抗体表达
- 抗体人源化
-
 400-621-6806
400-621-6806 -
 13116038708(微信同号)
13116038708(微信同号) -
 周一至周五 8:30-18:00
周一至周五 8:30-18:00 -

-
 0
0
-





