告别传统SELEX周期长?毛细管电泳助力适配体快速筛选!
- 2026-05-06
- 110
一、概述
毛细管电泳(CE)作为一种高效的均相分离技术,能有效分离迁移速率差异显著的“靶标-寡核苷酸”复合物和未结合的寡核苷酸,还可在毛细管出口对“靶标-寡核苷酸”复合物进行精准的定时收集。这使得毛细管电泳-指数富集配体系统进化技术(CE-SELEX)能在游离溶液或模拟生物流体环境中实现靶标与寡核苷酸的相互作用,让二者以天然结构结合,有利于维持适配体性能的稳定性。
CE-SELEX是指SELEX技术中的分离步骤通过毛细管电泳完成。传统SELEX技术通常需要8-12轮筛选才能获得高亲和性适配体,操作繁琐且耗时长达4-6周甚至更久。此外,多数分离过程会引入固相介质(如亲和色谱中的固定相连接臂、磁珠、芯片等)。与之不同,毛细管电泳技术无需借助介质固定靶标或单链DNA,可在自由溶液中实现靶标-单链DNA复合物与游离单链DNA的高分辨率、快速分离,是一种高效的适配体筛选技术。通过1-4轮毛细管电泳筛选即可获得高亲和性适配体,大幅节省了筛选时间和成本。同时,毛细管电泳可同步实现靶标-单链DNA复合物与游离单链DNA的分离和检测,能对单链DNA序列的整体分布进行定量分析,克服了传统SELEX筛选的盲目性。已有研究表明,CE-SELEX的分离效率至少比传统固相筛选技术高两个数量级。
二、CE-SELEX筛选流程
(1)靶标-文库孵育:将ssDNA文库与靶标混合,在适宜条件下孵育,形成“靶标-ssDNA”复合物;
(2)毛细管电泳分离:通过毛细管电泳技术,依据复合物与游离ssDNA的迁移率差异实现二者分离;
(3)复合物收集:精准收集电泳分离后含“靶标-ssDNA”复合物的组分;
(4)ssDNA扩增富集:对收集的复合物中的ssDNA进行PCR扩增,制备次级富集库;
(5)富集文库纯化:上一轮PCR扩增产物经硅胶膜纯化柱完成为洗脱与纯化,为下一轮筛选做准备;
(6)多轮循环富集:重复步骤(1)-(5)进行3-8轮富集;逐轮可优化孵育时间、靶标浓度、缓冲液条件,逐步提高筛选压力,淘汰低亲和力、非特异性结合序列。
(7)建库测序:将最终洗脱产物通过NGS测序获取全部候选适配体的碱基序列。
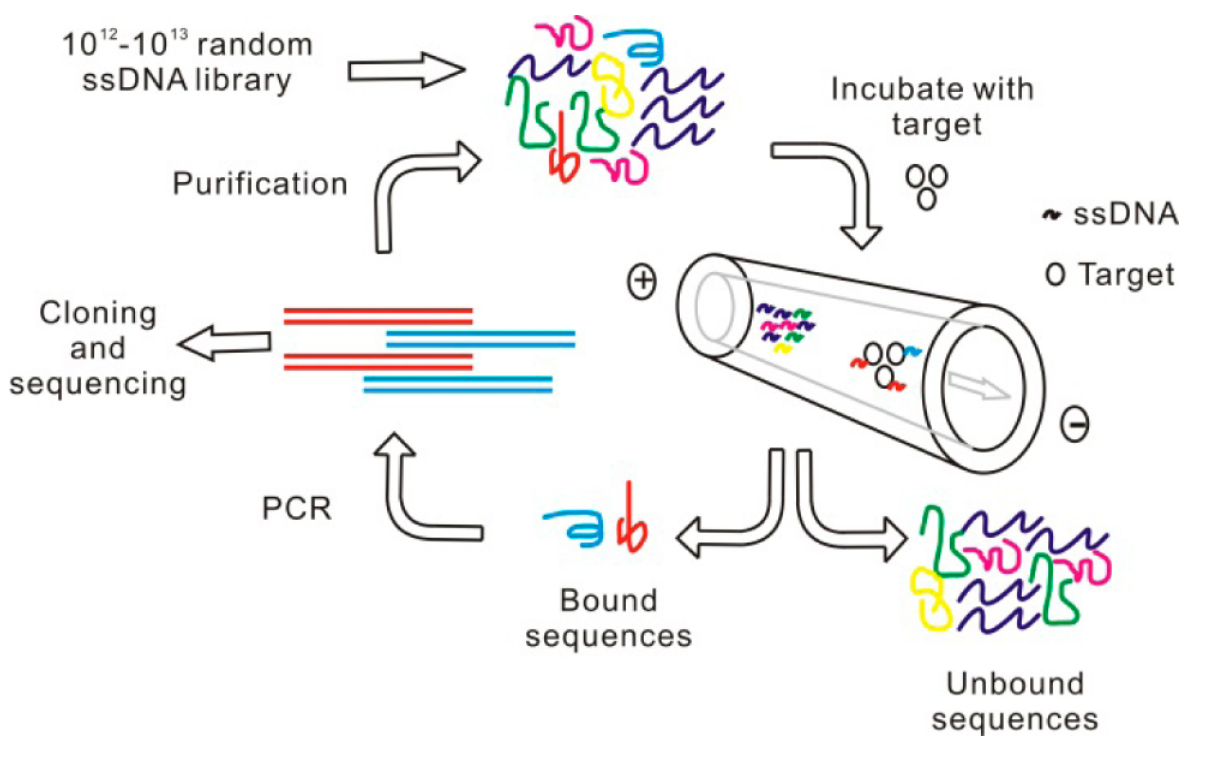
图1 CE-SELEX过程示意图(源自[1])
三、CE-SELEX靶标
根据筛选靶标类型的不同,CE-SELEX可划分为四种针对性的筛选亚型,依托毛细管电泳高效、快速、非固相亲和的分离特性,不同亚型可精准匹配从小分子到完整生物单元的多样化筛选需求,突破传统SELEX在不同靶标筛选中的固有局限。
(1)小分子靶标CE‑SELEX
适用于药物分子、代谢产物、生物毒素、环境小分子等低分子量靶标(100–5000Da),解决传统SELEX对小分子富集效率低、周期长的痛点,常用于小分子检测探针的快速筛选。
(2)大分子蛋白CE‑SELEX
适用于重组蛋白、酶、抗体、细胞因子等纯化蛋白靶标,依托自由溶液分离避免固相载体非特异性吸附,适合高亲和力蛋白适配体的高效富集。
(3)细胞/微生物CE‑SELEX
适用于活肿瘤细胞、细菌、病毒等完整生物靶标,无需靶标纯化,直接在天然膜环境下筛选,多用于肿瘤诊断、病原检测相关适配体开发。
(4)离子/无机复合物CE‑SELEX
适用于金属离子、无机小分子、配位化合物等无生物活性靶标,为环境监测、重金属检测领域提供高效适配体筛选路径。
四、CE-SELEX常见类型
传统SELEX方法存在筛选周期长、非特异性结合多、富集效率偏低等短板,而将毛细管电泳(CE)与SELEX技术相结合,依托毛细管电泳高分辨率、快速分离、样品耗量少的特性,开发出的CE-SELEX筛选体系,有效弥补了传统方法的缺陷,大幅提升了适配体筛选的效率与精准度。
(1)NECEEM (CZE-SELEX)
基于毛细管区带电泳(CZE),利用单链 DNA(ssDNA)、游离靶标及二者复合物在电场中迁移率的差异实现分离。在 t₁时刻将混合样品进样,t₂时刻通过电泳驱动,未结合 ssDNA、游离靶标与复合物因迁移速度不同形成不同区带,从而精准富集结合靶标的复合物组分。该方法是经典 CE-SELEX 范式,分离机制直观清晰,是早期毛细管电泳辅助适配体筛选的代表性方法,适合快速完成初始富集。
(2)LpH-CE-SELEX
低 pH(LpH)条件优化的 CE-SELEX,通过调控 pH 环境改变 ssDNA 与靶标的电荷状态或结合特性,放大复合物与游离组分的迁移率差异。t₁时刻进样后,在低 pH 电场中实现高效分离,t₂时刻收集复合物区带以提升富集特异性。借助 pH 调控减少非特异性结合,适配对 pH 敏感的靶标或适配体筛选场景,提升结合选择性。
(3)Non-SELEX
突破传统 SELEX 多轮扩增流程,通过多轮(Round 1、Round 2)毛细管电泳分离直接富集高亲和力复合物。每轮电泳中,复合物与游离 ssDNA、靶标被分离,省略 PCR 扩增等步骤,直接从初始文库中逐步筛选出高亲和力适配体。大幅缩短筛选周期,避免 PCR 扩增引入的序列偏差,适合快速获得高亲和力适配体。
(4)scCE-SELEX
单链构象敏感 CE-SELEX(scCE),利用 ssDNA 不同构象的迁移率差异,结合靶标后构象变化进一步放大分离差异。t₁时刻进样后,t₂时刻通过电泳将不同构象的 ssDNA、靶标及复合物分离,富集结合靶标的特定构象适配体。聚焦构象依赖的结合特异性,适合筛选构象敏感型适配体,适配结构特异性要求高的靶标。
(5)ssCE-SELEX
单链优化 CE-SELEX(ssCE),针对 ssDNA 分离条件进行优化,通过电场驱动使未结合 ssDNA、靶标与复合物在毛细管中形成清晰区带。t1时刻进样后,t2时刻高效分离并精准收集复合物区带,提升富集效率。简化单链分离步骤,提升筛选通量,适合高通量适配体筛选场景。
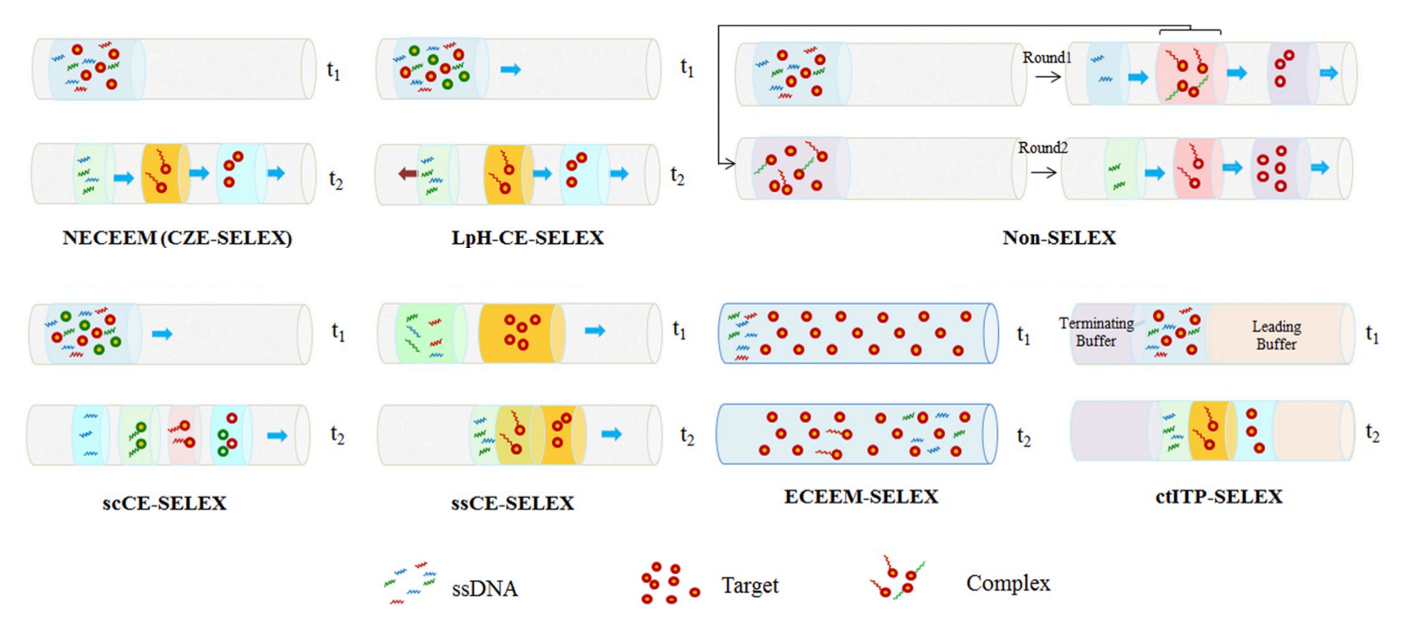
图2 基于毛细管电泳的多种SELEX模式(源自[2])
五、应用前景
基于CE-SELEX高效、快速的独特优势,该技术将靶标-核酸相互作用、高效分离与亲和选择集成于毛细管电泳平台,实现了“筛选-表征-应用”的一体化流程,极大提升了功能性核酸适配体的获取效率与成功率,使在临床诊断、靶向治疗、生物传感及环境监测等多个应用领域展现出巨大潜力。
(1)临床诊断与即时检测
CE-SELEX可大幅缩短针对疾病标志物(如循环肿瘤细胞、外泌体及自身抗体)的适配体筛选周期,满足临床样本动态监测与即时检测对时间敏感性的严苛要求。筛选所得适配体经毛细管电泳平台直接完成亲和力表征与特异性验证,实现“筛选-鉴定-应用”一体化流程,为开发高灵敏度、低成本的快速诊断试剂盒提供可靠分子工具。
(2)药物研发与靶向治疗
针对传统技术难以筛选的小分子药物、膜蛋白受体等靶标,CE-SELEX通过其高分辨率分离能力有效富集高亲和力适配体,可用于药物递送系统的靶向修饰或作为拮抗剂阻断关键信号通路。该技术也为复杂生物样品中活性成分的快速筛选提供了新策略,助力新药发现与精准医疗。
(3)生物传感与环境监测
结合毛细管电泳的高通量特性,CE-SELEX筛选的功能核酸可集成至微流控芯片或电化学传感器,实现对重金属离子、毒素及病原体的快速现场检测,在食品安全、环境监控等领域具有广阔的应用前景。
卡梅德依托成熟的噬菌体展示平台,能够构建库容高达10^13/mL的超高通量多肽或抗体文库,经过多轮生物淘选后可提供多达10^5个经严格验证的有效多肽或抗体序列。我们提供从靶标蛋白表达纯化、CE或噬菌体筛选、NGS测序到SPR/BLI亲和力验证的一站式服务,能够针对蛋白、小分子及细胞等复杂靶标定制个性化策略,交付pM至nM级别的高亲和力候选适配体,为诊断试剂开发与靶向药物递送提供坚实的技术支撑。
[1]YangJ,BowserMT.Capillaryelectrophoresis-SELEXselectionofcatalyticDNAaptamersforasmall-moleculeporphyrintarget.AnalChem.2013;85(3):1525-1530.
[2]ZhuC,YangG,GhulamM,LiL,QuF.Evolutionofmulti-functionalcapillaryelectrophoresisforhigh-efficiencyselectionofaptamers.BiotechnolAdv.2019;37(8):107432.
[3] Yang G, Tian W, Hu Y, et al. Real-time visualization of "small Molecules-ssDNA" complexes for aptamer screening based on online competition CE-SELEX. Talanta. 2025;284:127199.
-
 400-621-6806
400-621-6806 -
 3599163699
3599163699 -
 周一至周五 9:00-18:00
周一至周五 9:00-18:00 -

-
 0
0
-





