CD152/CTLA-4作用机制与FDA批准检查点抑制剂的成功应用
- 2026-05-09
- 14
CTLA-4(CD152)是免疫球蛋白超家族成员之一,其分子结构与共刺激因子CD28具有着高度的同源性。该蛋白主要表达于活化T细胞的表面,而在调节性T细胞(Treg)中呈组成性高表达状态。CTLA-4与CD28共用CD80、CD86两种配体,但却发挥着与CD28相反的免疫抑制作用,且结合亲和力显著高于CD28,因此在免疫调控中发挥着重要作用。
CTLA-4参与维持机体的免疫平衡与自身的免疫耐受,故其功能的缺陷会引发严重的自身免疫疾病。而使用CD152抗体阻断CTLA-4能够解除这种免疫抑制,增强机体针对肿瘤的免疫应答反应,这一机制推动着CTLA-4成为了首个成功被临床转化的免疫检查点靶点。
一、CTLA-4的多重抑制机制
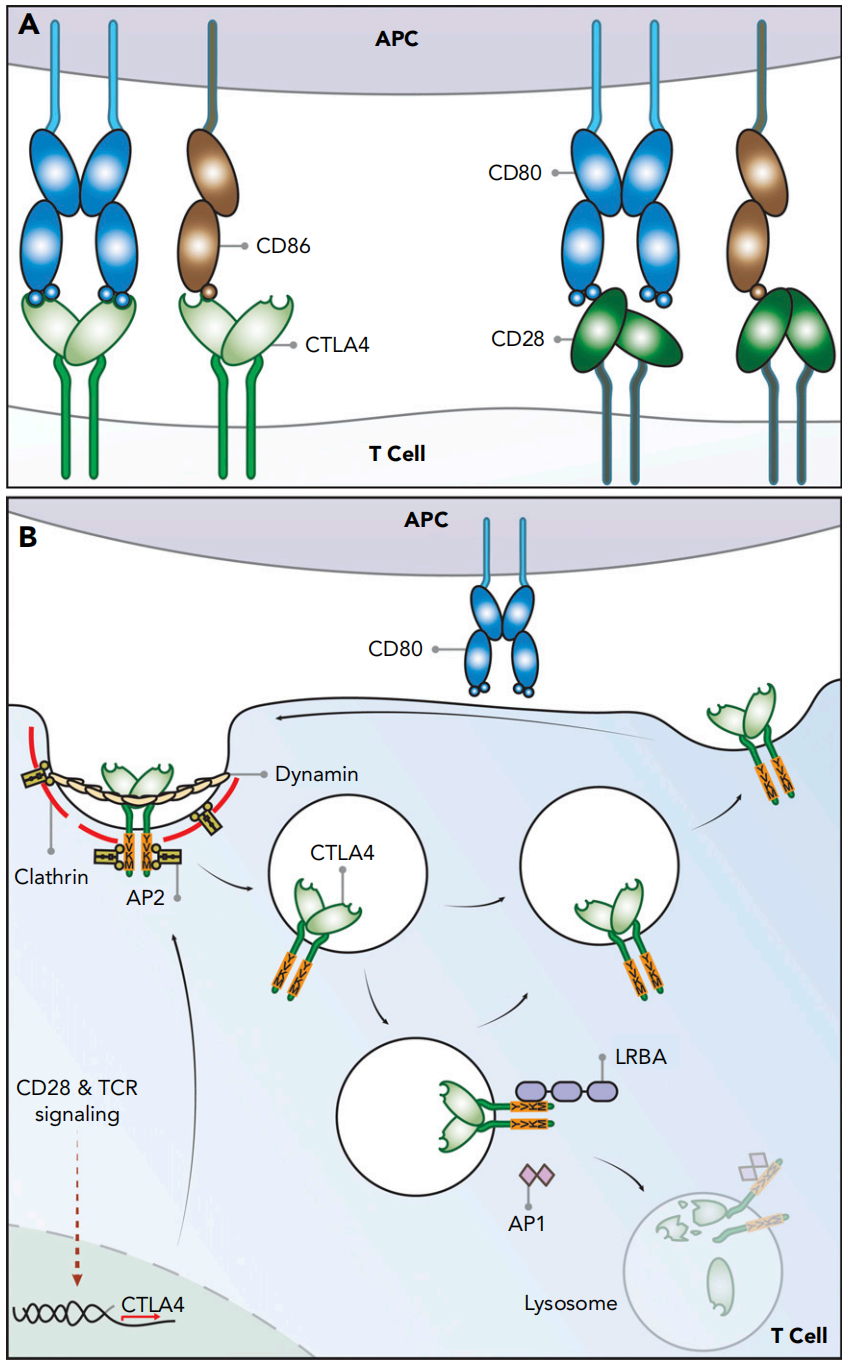
图1 CTLA-4细胞生物学示意图
CTLA-4介导免疫抑制的机制是多元且精密的,主要可归纳为以下两点:
1. 竞争性拮抗与信号干扰:CTLA-4对CD80/CD86具有高结合亲和力,可在免疫突触区域与CD28争夺结合位点,限制CD28对共刺激信号的识别接收,进而抑制T细胞活化。这一机制可调控机体免疫反应强度,并决定了T细胞活化信号水平。在这个过程中,CTLA-4自身不传递活化信号,仅通过物理占位阻断胞外共刺激信号向细胞内部的传递。
2. 主动清除配体的转内吞作用:CTLA-4并非仅进行被动结合竞争,还可主动剥离抗原呈递细胞(APC)膜表面配体。通过“转内吞”过程,表达CTLA-4的T细胞可捕获并降解APC表面的CD80/CD86蛋白,这种胞外作用模式赋予了CTLA-4高效的免疫抑制能力,即便是在配体高表达的条件下,仍可阻断共刺激信号的传递。此外,CTLA-4还可向TCR信号复合体募集SHP-2、PP2A等磷酸酶分子,直接抑制胞内下游信号传导,从胞内层面增强整体的免疫抑制作用。
二、FDA批准的抗CTLA-4单抗
CTLA-4在机体自身免疫耐受维持中具备着核心功能,这一特性使其成为肿瘤免疫治疗的重要研究靶点。CTLA-4基因敲除小鼠可发生致死性自身免疫淋巴增殖性病变,这一结果直接证明了阻断CTLA-4功能可解除免疫耐受,提高机体抗肿瘤免疫应答水平。
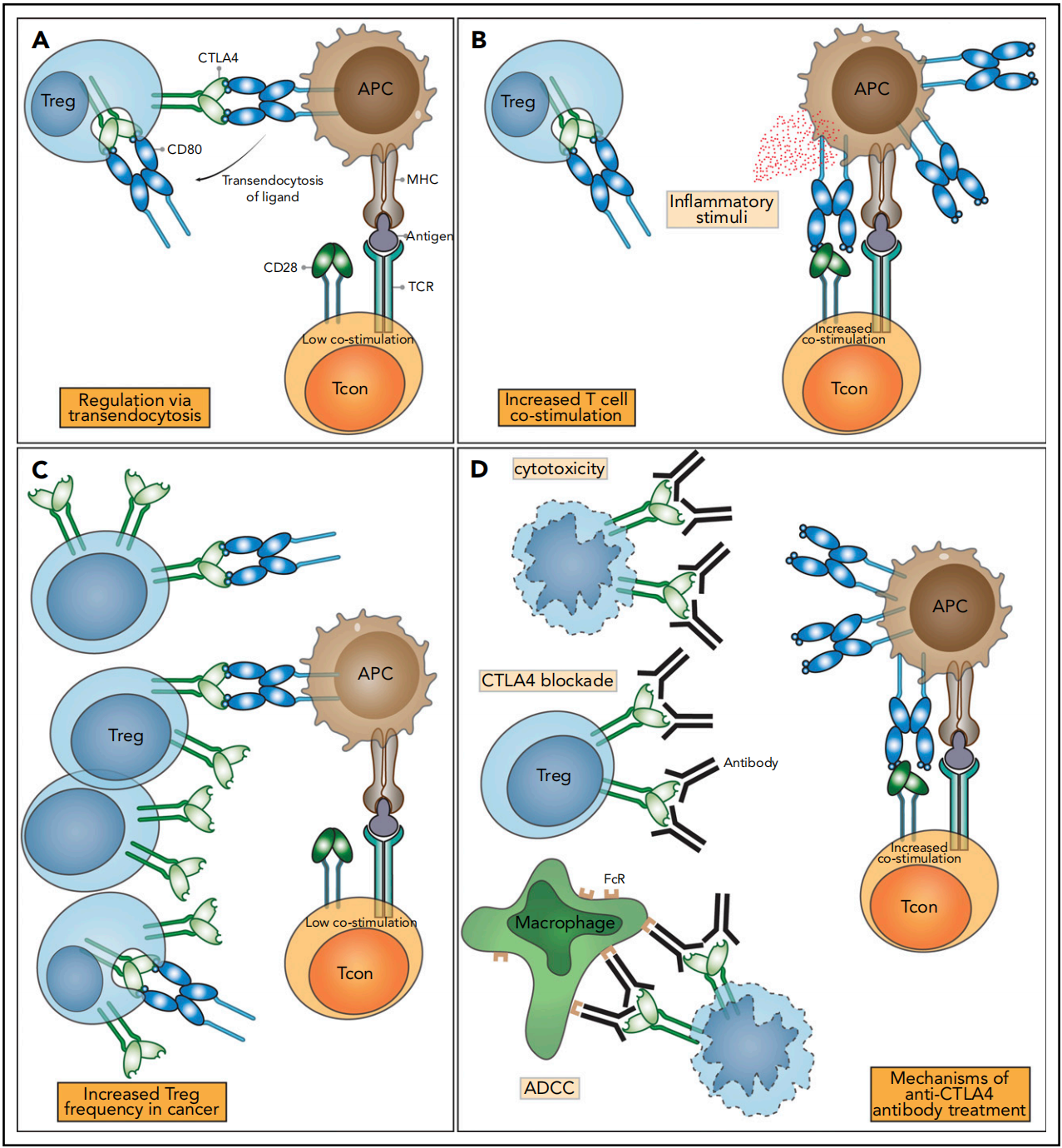
图2 CTLA-4功能及免疫检查点阻断的影响
基于上述研究基础,靶向CTLA-4的单克隆抗体药物应运而生,其中伊匹木单抗(Ipilimumab)成为了应用效果突出的代表性药物。
Ipilimumab是一种全人源IgG1单克隆抗体,可特异性地结合CTLA-4,阻断其与配体CD80/CD86的相互作用。这种阻断带来了多方面的抗肿瘤效应:
Ø 增强效应T细胞功能:通过解除CTLA-4介导的阻断,CD28共刺激信号可以得到恢复,促进了初始T细胞的活化、增殖以及向效应T细胞的分化,尤其是CD8+细胞毒性T细胞。
Ø 重塑肿瘤微环境:Treg细胞是肿瘤微环境中免疫抑制的重要角色,它们通过高表达CTLA-4来抑制效应T细胞。Ipilimumab可以阻断Treg细胞的抑制功能,同时,其抗体的Fc段还可介导抗体依赖的细胞介导的细胞毒性作用(ADCC),有效清除肿瘤局部的Treg细胞,从而逆转免疫抑制微环境。
2011年,一项III期临床试验(MDX010-20)证明了Ipilimumab显著可延长晚期黑色素瘤患者的总生存期,自美国FDA正式批准其用于治疗晚期黑色素瘤,开启了免疫检查点抑制剂应用时代,并首次证实靶向CTLA-4的CD152抗体在恶性肿瘤治疗中具备重要应用价值。CD152抗体临床应用为肿瘤患者提供了新的治疗手段,同时也验证了增强机体免疫功能实现抗肿瘤治疗的科学可行性。
三、CTLA-4靶向治疗的挑战与未来方向
尽管Ipilimumab的成功开启了肿瘤免疫治疗的新纪元,但在临床应用中仍存在着多项局限。单药使用客观应答率仅10%-20% 并伴随高比例免疫相关不良反应,包括结肠炎、皮肤红斑、垂体炎等。这正是因为,阻断CTLA-4会打破机体免疫平衡,激活自身反应性T细胞,并损伤正常组织。
为了提升药物的治疗效果并降低其毒性,研究人员探索了多种联合用药方案。其中,Ipilimumab与PD-1抑制剂的联合使用获得了良好疗效。CTLA-4参与T细胞早期活化调控;而PD-1在肿瘤微环境中限制效应T细胞活性。这两种药物的联合可通过启动与效应的双重通路激活肿瘤局部免疫反应,将免疫惰性肿瘤转化为免疫响应型肿瘤,整体提升机体的抗肿瘤应答水平。
该联合用药方案已获美国FDA批准,用于黑色素瘤、肾细胞癌等多种恶性肿瘤临床治疗。
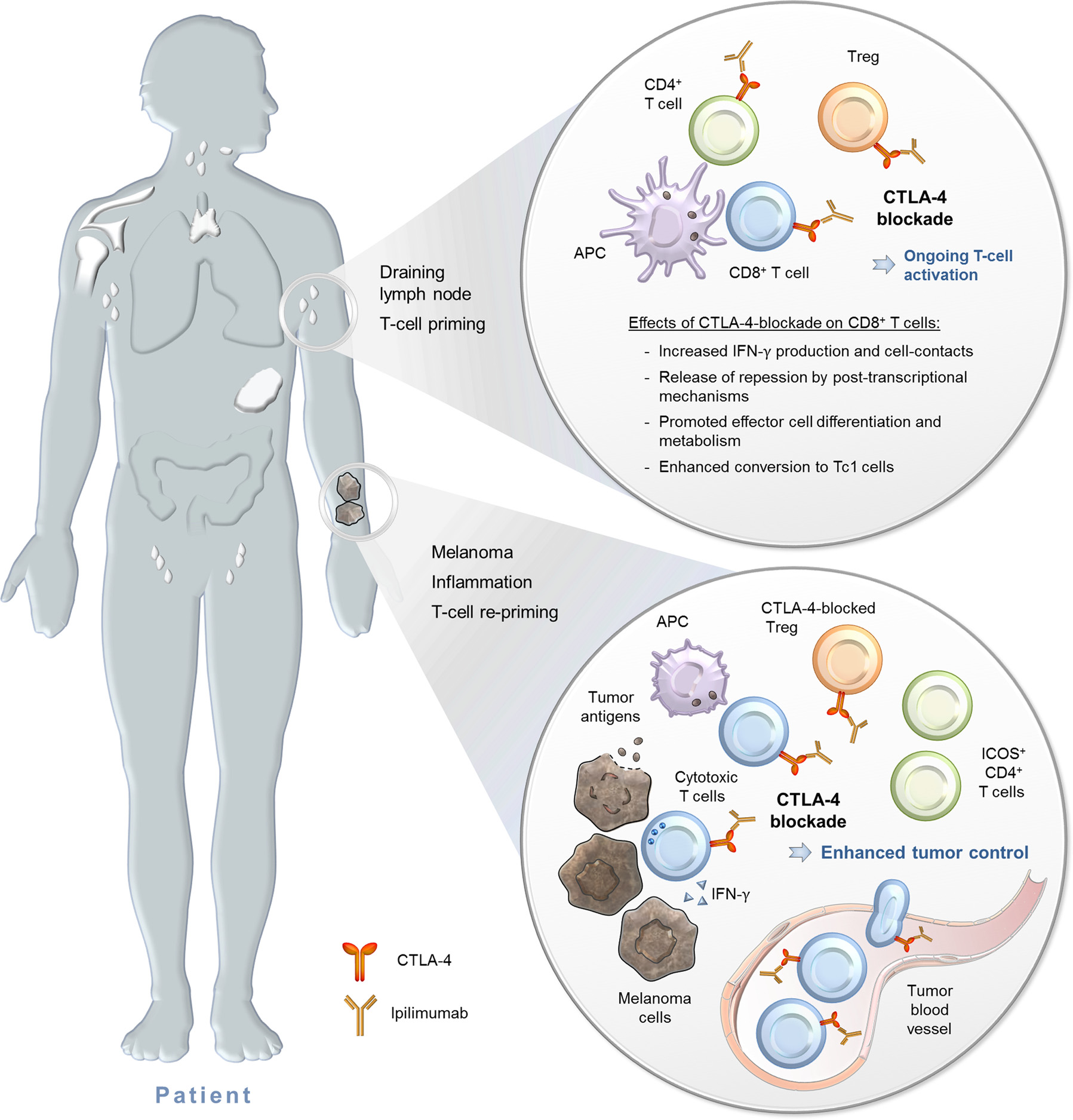
图3 黑色素瘤患者CTLA-4阻断模型
对CTLA-4蛋白空间结构的深入研究推动着多种CD152抗体及新型药物制剂的开发。例如,改造抗体的Fc段可提升抗体在肿瘤微环境中对Treg的ADCC清除效率、优化药物的代谢特性,成为了新一代抗体的研发重点。同时,CTLA-4抑制剂与化疗、放疗、溶瘤病毒等疗法的联合应用可在安全范围内提升抗肿瘤疗效,成为了当前临床研究的重点内容。
CTLA-4作为首个成功靶向的免疫检查点分子,改变了肿瘤治疗模式,为后续免疫靶点开发提供了重要实践依据。卡梅德生物凭借在蛋白表达、抗体开发等领域的技术积累,持续为疾病相关靶点的机制研究与药物研发提供关键支持,拥有抗体定制平台、蛋白表达平台、纳米抗体平台等多个平台,高效推动基础发现向临床转化迈进,为肿瘤免疫治疗带来更多可能。
CTLA-4(CD152)靶点相关产品包括:
Protein | |||
Catalog Number | Product Name | Sequence | Expression System |
KMP2860 | Met1-Phe162 | HEK293 | |
KMP2862 | Met1-Phe162 | HEK293 | |
Antibod | |||
Catalog Number | Product Name | Molecular Name | Application |
YR1160 | Tremelimumab | IF, IP, Neut, FuncS, ELISA | |
YR1551 | Zalifrelimab | WB | |
[1] Rowshanravan B, Halliday N, Sansom DM. CTLA-4: a moving target in immunotherapy. Blood. 2018 Jan 4;131(1):58-67.、
[2] Lingel H, Brunner-Weinzierl MC. CTLA-4 (CD152): A versatile receptor for immune-based therapy. Semin Immunol. 2019 Apr;42:101298.
[3] Hosseini A, Gharibi T, Marofi F, Babaloo Z, Baradaran B. CTLA-4: From mechanism to autoimmune therapy. Int Immunopharmacol. 2020 Mar;80:106221.
[4] Carreno BM, Bennett F, Chau TA, Ling V, Luxenberg D, Jussif J, Baroja ML, Madrenas J. CTLA-4 (CD152) can inhibit T cell activation by two different mechanisms depending on its level of cell surface expression. J Immunol. 2000 Aug 1;165(3):1352-6.
*CTLA-4(CD152)靶点相关常见问题汇总:
Q1:CTLA-4结构异常与自身免疫疾病的关联是什么?
CTLA-4作为免疫球蛋白超家族成员,其分子结构的完整性直接影响免疫调控功能。若其结构出现异常,会导致与CD80、CD86配体的结合能力异常,或无法正常募集磷酸酶分子,进而丧失有效的免疫抑制作用。这种功能缺陷会打破机体免疫平衡,使自身反应性T细胞过度活化,攻击正常组织和细胞,最终引发多种严重自身免疫疾病。此外,CTLA-4基因的多态性也与自身免疫疾病存在关联,部分变异会增加患病风险,其结构异常的程度直接决定了自身免疫疾病的发病概率和严重程度。
Q2:CTLA-4的抑制机制对肿瘤免疫治疗有哪些核心启发?
明确靶向阻断的核心思路,CTLA-4通过竞争性结合配体和主动清除配体实现免疫抑制,启发研究人员通过抗体阻断其与配体的相互作用,解除免疫抑制,释放机体抗肿瘤免疫潜力,为免疫检查点抑制剂的研发提供核心方向。
揭示免疫调控的精密性,其胞内与胞外双重抑制机制表明,靶向治疗需兼顾阻断配体结合和抑制胞内信号传导,才能实现更高效的免疫激活,为新型制剂的分子设计提供理论支撑。
提示治疗安全性边界,CTLA-4的免疫抑制作用是维持自身耐受的关键,启发临床治疗中需平衡免疫激活与免疫平衡,避免过度阻断引发严重不良反应。
Q3:新型CTLA-4制剂相比传统单抗有哪些核心优势?
靶向性更精准,新型制剂通过分子设计实现对肿瘤微环境的选择性作用,可特异性清除肿瘤局部的Treg细胞,避免对正常组织中Treg细胞的抑制,大幅降低免疫相关不良反应的发生率,提升治疗安全性。
疗效更显著,部分新型制剂通过优化结合亲和力,可更高效阻断CTLA-4与配体的相互作用,同时增强对胞内信号传导的抑制干扰,提升免疫激活效率,尤其对PD-1耐药患者展现出良好的治疗潜力。
适用范围更广,新型制剂可与化疗、放疗、溶瘤病毒等多种疗法协同作用,突破传统单抗单药适用范围有限的局限,为不同类型、不同分期的肿瘤患者提供个性化治疗方案。
Q4:CTLA-4在Treg细胞中的高表达对免疫调控有何意义?
CTLA-4在Treg细胞中呈组成性高表达,是Treg细胞发挥免疫抑制功能的核心支撑,对维持机体免疫平衡具有重要意义。Treg细胞作为免疫抑制的关键细胞,通过高表达CTLA-4,可优先与抗原呈递细胞表面的CD80、CD86配体结合,一方面竞争性阻断CD28的共刺激信号,抑制效应T细胞活化;另一方面通过转内吞作用主动清除配体,减少共刺激信号的传递,进一步增强免疫抑制效果。这种表达模式可帮助Treg细胞精准调控免疫反应强度,避免免疫过度激活引发自身免疫疾病,同时在肿瘤微环境中,Treg细胞表面的CTLA-4也是肿瘤免疫逃逸的重要机制之一,为靶向治疗提供了关键靶点。
Q5:CTLA-4靶向治疗在临床应用中面临哪些具体局限及应对思路?
单药疗效有限,客观应答率较低,应对思路主要是探索联合治疗方案,除与PD-1抑制剂联合外,还可与化疗、放疗、溶瘤病毒等疗法结合,通过协同作用提升抗肿瘤疗效,扩大应答人群。
免疫相关不良反应发生率高,应对思路包括优化药物分子设计,提升靶向性以减少全身毒性,同时完善不良反应分级管理体系,早期识别、及时干预,降低不良反应对患者生活质量的影响。
部分患者存在治疗耐药,应对思路是深入研究耐药机制,开发新型CTLA-4制剂,如pH敏感性抗体、双抗产品等,突破耐药瓶颈,同时结合患者个体差异,制定个性化治疗策略。
-
 400-621-6806
400-621-6806 -
 3599163699
3599163699 -
 周一至周五 9:00-18:00
周一至周五 9:00-18:00 -

-
 0
0
-





