骆驼源抗体的人源化革新:用于治疗的VHH纳米抗体工程
- 2026-05-06
- 9
一、VHH纳米抗体的核心特性
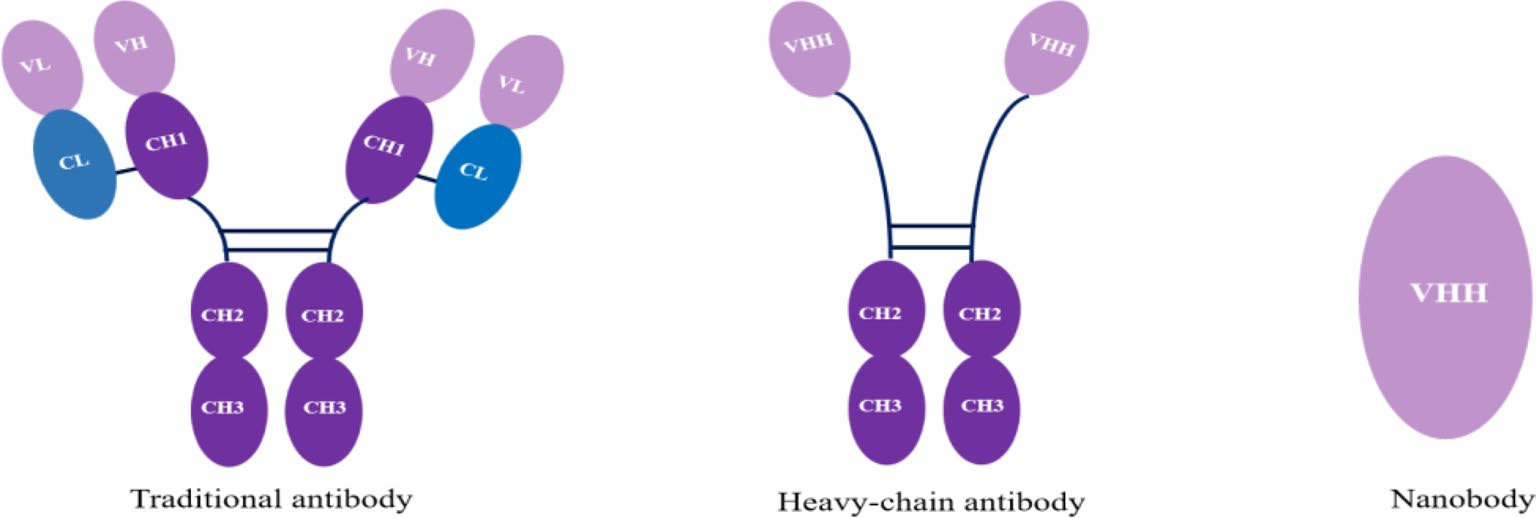
图1 传统抗体、重链抗体和纳米抗体的结构图
骆驼源单域抗体(VHH)是纳米抗体的关键功能组成部分,是骆驼科动物重链抗体中仅含重链可变区的特殊分子,分子量12-15kDa,约为常规单克隆抗体的十分之一,其紧凑的分子结构使其在生物医疗应用领域具备极高的开发价值:
Ø 抗原结合特异性突出,CDR3区域更长且构象灵活,能靶向传统抗体难以触及的抗原隐蔽表位;
Ø 结构稳定性优异,框架区(FR)特有的Hallmark 残基和非经典二硫键,维持CDR3的生物活性构象;
Ø 生产改造便捷,可通过原核表达系统高效制备,易于进行多价化、双特异性融合等工程改造。
然而,骆驼源VHH与人IGHV3家族基因具有约80%的序列同源性,骨架区域的外源氨基酸残基仍可能引发抗药抗体(ADA)应答。因此,人源化革新是VHH抗体实现临床转化的核心步骤,需要在维持抗原结合活性的同时最大程度降低免疫原性。
二、VHH噬菌体展示技术
VHH噬菌体展示技术作为VHH抗体发现的核心工具之一,凭借着高通量、高特异性的优势,成为了连接骆驼免疫与临床候选分子的关键桥梁,其核心流程包括:
1. 免疫文库构建:骆驼经目标抗原免疫后,从外周血单核细胞(PBMC)提取RNA,反转录获得cDNA,扩增VHH编码序列并与噬菌体外壳蛋白基因融合,构建多样性可达108以上的VHH噬菌体展示文库。
2. 抗原亲和筛选:通过多轮“结合-洗涤-洗脱”循环,富集特异性结合抗原的VHH噬菌体克隆。
3. 序列鉴定与验证:对富集克隆测序,获得VHH基因序列,经原核表达制备重组VHH抗体并验证关键特性。
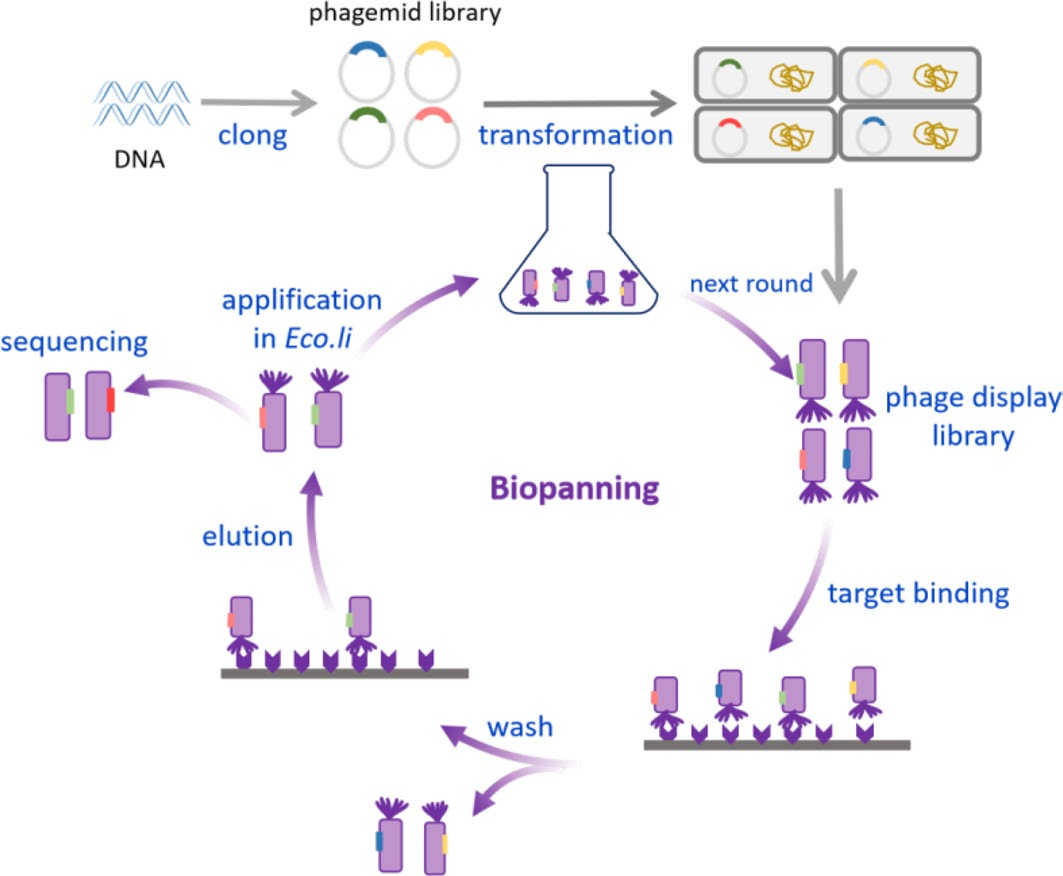
图2 噬菌体展示技术示意图
相较于传统杂交瘤技术,该技术将筛选周期从数月缩短至数周,可直接获得基因序列便于后续人源化改造,已广泛应用于肿瘤、自身免疫病等领域的VHH抗体筛选。
三、技术挑战与精准解决方案
VHH抗体的人源化需平衡免疫原性降低与生物活性保留,面临结构功能保全、亲和力维持等核心挑战。
1. 核心技术挑战
Ø 关键结构元件功能平衡:Hallmark残基和非经典二硫键参与维持VHH结构稳定与CDR构象,改造需精准把控;
Ø 亲和力保留难题:Vernier区残基人源化可能改变CDR与抗原结合模式,导致亲和力下降;
Ø 免疫原性控制:框架区异源残基需修饰,但过度改造可能引发结构不稳定。
2. 新一代人源化策略
Ø 框架区定向改造:以人类IGHV3-23*01为模板,优先保留Hallmark残基和非经典二硫键相关位点,仅修饰非关键异源残基,可将人源化程度提升至90%以上;
Ø 结构引导定点突变:借助AlphaFold2预测复合物结构,结合分子动力学模拟,替换与抗原结合无关的异源残基;
Ø 组合文库筛选策略:将高亲和力VHH的CDR3序列与人类化框架区组合,构建半合成人源化文库,通过VHH噬菌体展示快速筛选优化变体。
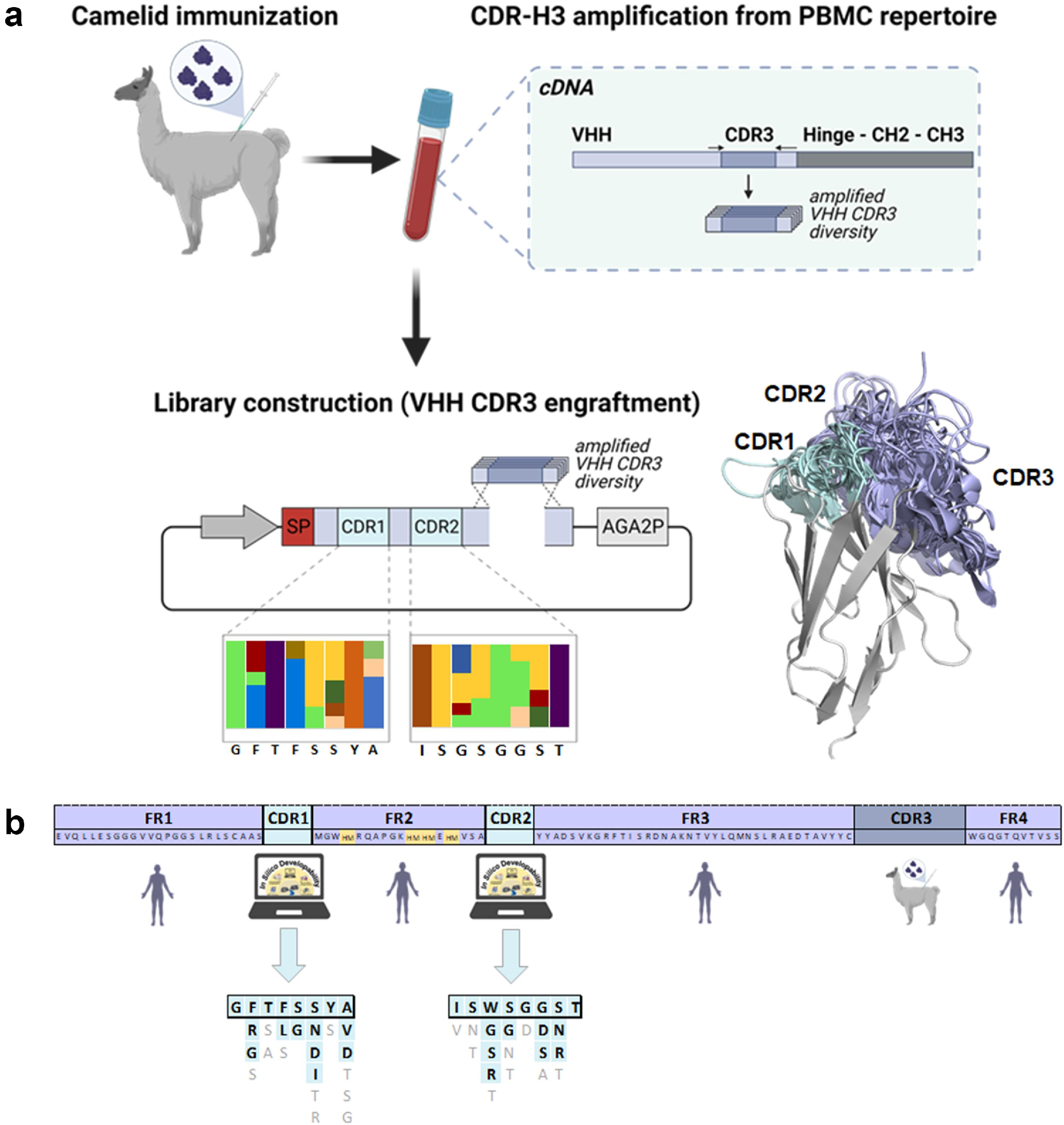
图3 基于骆驼免疫的人源化 VHH CDR3 移植文库构建流程
四、人源化VHH的临床转化与应用进展
人源化优化的VHH纳米抗体在临床转化中已经取得了明显进展,可用于肿瘤免疫治疗与自身免疫疾病等领域,靶向NK细胞受体NKp30的人源化VHH 抗体能够激活NK细胞毒性作用,并在实体瘤治疗中表现出较强的肿瘤杀伤效果。
在药代动力学优化方面,通过与血清白蛋白结合域融合或PEG修饰,可将VHH抗体的体内半衰期从数小时延长至数天,双特异性VHH抗体可同时识别肿瘤抗原与免疫检查点,实现肿瘤靶向与免疫激活的协同作用。
产业化层面,VHH抗体可通过原核表达系统高效制备,生产成本仅为传统抗体的1/2至1/3,小分子结构使其能够穿透肿瘤组织与血脑屏障等传统抗体难以进入的区域,Caplacizumab 等VHH相关药物已获批上市,证明了其临床应用价值与产业潜能。
五、多技术融合驱动的VHH革新
VHH纳米抗体的人源化革新仍在持续推进,未来将聚焦多维度优化:
1. 人工智能辅助设计:通过分析大规模VHH序列与结构数据,精准预测突变位点功能影响,减少实验筛选工作量;
2. 新型产品形式开发:多价化、多特异性VHH融合蛋白成为研发热点,如三特异性VHH抗体可同时靶向肿瘤抗原、T细胞和NK细胞表面分子,实现多效协同治疗;
3. 罕见病治疗应用:借助VHH噬菌体展示技术的高通量优势,加速罕见病相关靶点的VHH抗体研发。
VHH纳米抗体的人源化革新打破了骆驼源抗体的免疫原性壁垒,VHH噬菌体展示技术与精准人源化策略的有机结合,构建了从VHH发现到临床转化的完整技术链条。卡梅德科技(KMD Bioscience)拥有经验丰富的重组抗体制备团队,可提供纳米抗体文库构建、噬菌体展示文库筛选、VHH抗体人源化等服务,为客户制备理想的VHH抗体。
常见问题
Q1:纳米抗体作为外来蛋白质,其免疫原性如何?在临床治疗中如何应对这一问题?
尽管纳米抗体源自骆驼科动物,其氨基酸序列与人类存在差异,因此在人体内确实存在引发免疫反应的风险,可能导致产生抗药物抗体,影响疗效和安全性。这是其临床转化中必须谨慎评估的关键问题。
为应对这一挑战,科研与产业界已发展出多重有效策略:
Ø 人源化改造:这是最核心的手段。通过分子生物学技术,将纳米抗体框架区中非关键的、可能被人体免疫系统识别为“异己”的氨基酸残基,替换为人类抗体中常见的相应残基。这能显著降低其免疫原性,同时尽可能保留其高亲和力和稳定性。
Ø 生成完全人源的纳米抗体:虽然技术挑战更大,但研究者正尝试从人源天然单域抗体库中筛选VH片段,或利用转基因小鼠平台生成完全人源的类似物,以期从源头上解决免疫排斥问题。
Ø 全面的临床评估:在药物开发过程中,会通过体外免疫原性预测模型和体内实验进行早期风险评估。在临床试验阶段,则会严密监测患者体内抗药物抗体的产生情况及其对药代动力学、药效学和安全性的实际影响。
Q2:纳米抗体在生产制造上与传统抗体相比有何优势?
纳米抗体的生产兼具了部分小分子和抗体的特性,形成了独特且更具成本效益的制造路径。其核心优势在于卓越的可表达性和稳定性。
由于其结构简单、不含复杂的链间二硫键和糖基化修饰,纳米抗体可以在成本低廉的大肠杆菌或酵母等微生物系统中进行高效、高产量地表达。这彻底避免了传统抗体必须使用哺乳动物细胞(如CHO细胞)的复杂、昂贵且耗时的生产过程。此外,它们卓越的物理化学稳定性使其在发酵、纯化和储存过程中更不易降解和聚集,从而提高了最终产品的得率和均一性。
当然,挑战也同样存在,例如因其分子量小,在采用常规层析纯化时需要更精细的工艺控制。但总体而言,纳米抗体在规模化生产上具有显著的成本和效率优势,更易于实现大规模、低成本的生产,这对降低未来药物的价格至关重要。
Q3:除了已提到的疾病,纳米抗体在哪些其他脑部疾病中有应用潜力?
纳米抗体平台的灵活性使其在多种中枢神经系统疾病中具有广阔的应用前景,远超阿尔茨海默病和精神分裂症。
1. 在帕金森病领域,可以设计靶向α-突触核蛋白聚集体的纳米抗体,用以抑制其病理性纤维的形成和细胞间传播。
2. 对于脑肿瘤,纳米抗体可作为“特洛伊木马”,通过靶向血脑屏障上的受体主动进入大脑,并进一步与靶向肿瘤特异性抗原的纳米抗体组成双特异性药物,将抗癌效应精准递送至胶质母细胞瘤等肿瘤内部。
3. 在疼痛管理领域,可以开发靶向疼痛通路中关键受体(如特定亚型的阿片受体)的纳米抗体,通过变构调节等方式实现精准镇痛,同时有望避免成瘾等副作用。这些探索性研究正在蓬勃发展,预示着纳米抗体有望成为中枢神经系统药物开发的通用型强大工具。
Q4:什么是噬菌体展示技术?它在纳米抗体制备中为何如此重要?
噬菌体展示是纳米抗体筛选最核心、最成熟的技术平台。其原理是将编码数十亿种不同纳米抗体的基因片段,与编码噬菌体(一种病毒)外壳蛋白的基因融合,使得每一个噬菌体颗粒表面都能“展示”一种独特的纳米抗体,而其内部则包含着该纳米抗体的基因。
这个过程如同制作一个分子级别的“身份证”库。当我们需要寻找能结合特定靶点(如新冠病毒的S蛋白)的纳米抗体时,只需让这个庞大的噬菌体库与固定的靶点接触。那些无法结合的噬菌体会被洗掉,而能够特异性结合的极少数“精英”则被保留下来。这些被筛选出的噬菌体经过感染细菌进行扩增后,可以开始下一轮更严格的筛选。通常经过3-5轮的“吸附-洗涤-洗脱-扩增”循环,与靶点亲和力最高、特异性最强的纳米抗体就会被富集出来。最后,通过测序展示该纳米抗体的噬菌体基因,就能获得其精确的氨基酸序列,用于后续生产。
Q5:获得纳米抗体序列后,如何大规模生产?主要挑战是什么?
一旦通过筛选获得理想纳米抗体的基因序列,大规模生产通常使用微生物发酵系统,尤其是大肠杆菌。
其标准流程是:将纳米抗体基因克隆到表达载体中,然后转入经过优化的大肠杆菌工程菌株。在可控的发酵罐中,通过诱导剂(如IPTG)启动基因表达,菌体便会大量合成纳米抗体。随后,通过破碎菌体、收集上清或包涵体,再经过一系列层析纯化步骤(如亲和层析、离子交换层析等),即可获得高纯度的纳米抗体产品。
-
 400-621-6806
400-621-6806 -
 3599163699
3599163699 -
 周一至周五 9:00-18:00
周一至周五 9:00-18:00 -

-
 0
0
-





