拆解蛋白质纯化过程中的核心作用力
- 2026-05-12
- 11
一、分子作用力本质
重组蛋白表达后的体系组分复杂,除目标蛋白外,还包含杂蛋白、核酸、小分子杂质等。蛋白分子表面分布着带电氨基酸、极性侧链与疏水残基,可产生多种非共价分子间作用力,这也是重组蛋白能够分离纯化的底层核心。与稳定性极强的共价键不同,分子间作用力属于弱相互作用,具备可逆、易调控的特点,可在不破坏蛋白肽链骨架的前提下完成分离,最大程度保留蛋白天然构象与生物活性。
蛋白纯化体系存在多种分子间作用力,主要包含静电作用、疏水作用、氢键与范德华力。各类分子作用力形成机制与作用强度具备差异化,可于蛋白分离阶段同步发挥作用。此外,缓冲液离子浓度、酸碱、环境温度等工艺参数的改变能够精准调节分子作用力大小,实现体系杂质的有效去除,同时减少蛋白聚合及空间结构破坏现象,保障重组蛋白提纯质量与生物学活性。
二、核心作用力机制
重组蛋白纯化依托静电作用、疏水作用、氢键及范德华力四类非共价弱作用力实现差异化分离。各类作用力独立发挥作用且互不替代,适配不同层析工艺场景,同时可通过缓冲液参数调控作用强度,在不破坏蛋白肽链骨架的前提下,完成杂质去除与目标蛋白富集,是重组蛋白制备的核心底层机制。
静电作用是离子交换层析的核心机制。受缓冲液pH与蛋白等电点差值影响,蛋白表面产生稳定净电荷,可与带电层析介质发生可逆吸附。工艺中通过调节盐浓度,利用游离盐离子竞争结合位点,实现蛋白吸附与梯度洗脱,主要用于发酵上清粗纯,去除核酸、水溶性杂蛋白等大批量杂质。
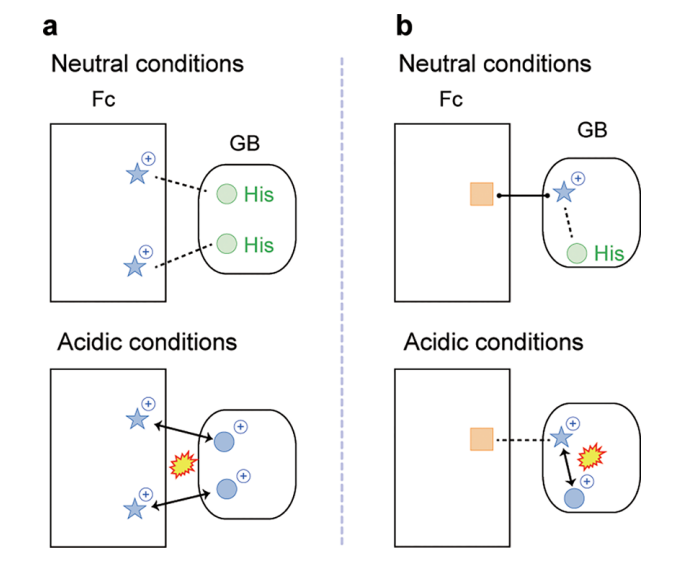
图1 蛋白质G B1结构域与IgG Fc区域分子间和分子内静电排斥作用的示意图
疏水作用专用于去除和目标蛋白电荷相近、难以通过离子交换分离的同源杂蛋白与微量聚集体,可在高盐脱水环境下与疏水介质结合,多用于重组蛋白精细纯化阶段。
氢键和范德华力可构成蛋白结合过程的辅助作用形式。蛋白极性侧链、水分子与介质官能团的相互作用能够提升层析吸附的结合专一性,保障蛋白分离阶段的区分能力。短程范围内产生的范德华力本身作用强度较弱,该类作用力的叠加积累可以固定蛋白质与层析介质的结合形态。此外,蛋白纯化流程内的四类分子作用力共同作用能够提高重组蛋白成品纯度并维持规模化制备阶段的结构稳定状态。
三、作用力维系蛋白稳态
在重组蛋白制备纯化流程中,各类分子间作用力除实现杂质分离外,也是维持蛋白空间构象与生物稳态的核心支撑。蛋白质的天然二级、三级构象,并非依靠刚性共价键固定,而是由静电作用、疏水作用、氢键等多种弱作用力相互制衡、协同维持。一旦分子间作用力失衡,蛋白极易发生构象舒展、结构解折叠,进而产生聚集、沉淀与活性丧失等问题。
纯化过程的环境参数会直接扰动作用力平衡,酸碱数值、离子浓度、环境温度的小幅变动可以改变蛋白质内外分子作用的稳定状态。其中强酸碱条件能够破坏电荷作用平衡,高盐环境会加快蛋白疏水区域的聚集行为。因此,蛋白提纯过程依靠微观分子作用完成不同组分拆分,同步实现各类微观作用力的动态调控。通过优化缓冲体系参数,可以维持分子间相互作用的稳定形态,减少蛋白降解与聚集概率,维持重组蛋白纯化后的结构完整性与生物活性。
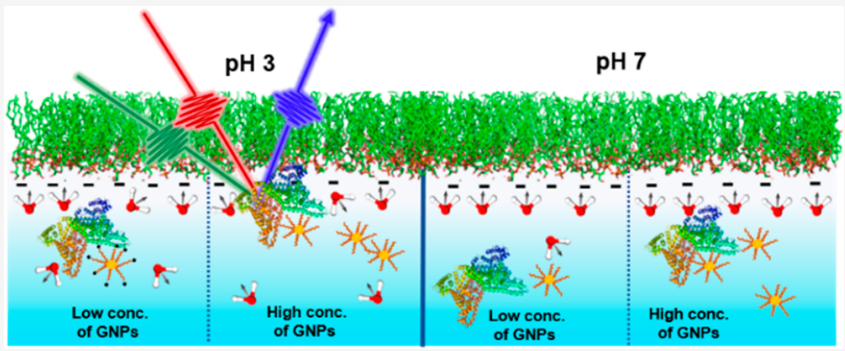
图2 pH值影响疏水和亲水纳米颗粒在空气-水和脂-水界面上对人血清蛋白的吸附
四、重组蛋白制备优化
重组蛋白制备与纯化的工艺优化,本质是对各类分子间作用力的精细化调控与组合运用。单一的静电分离或疏水分离难以去除全部杂质,且极易造成蛋白构象损伤、收率下降。根据目标蛋白的氨基酸特性、表面带电性与疏水特性,针对性搭配层析工艺,是提升制备质量的核心思路,也是重组蛋白工业化制备的关键要点。
工艺优化阶段是利用静电作用完成粗纯化除杂,再通过精准调控疏水作用力完成精细提纯,同时搭配适宜的缓冲液pH、盐浓度与温度,可长期维持分子作用平衡体系。该方案能够清除核酸杂蛋白等多种杂质物质,提升目标蛋白整体纯度,稳定蛋白空间构象,减少聚集变性。
卡梅德生物(KMD Bioscience)拥有成熟的蛋白制备平台,提供原核、酵母、昆虫杆状病毒及哺乳动物细胞四大主流技术平台,交付的重组蛋白、天然蛋白及特殊修饰蛋白具有高纯度、高活性、低内毒素和优异的批间一致性。基于噬菌体展示技术平台,以制备的高品质可溶蛋白为靶标,可构建多样化的多肽文库(7肽、12肽、环7肽等),通过生物淘洗筛选富集出与靶蛋白具有高亲和力的功能性多肽,为下游功能研究与应用开发提供可靠支持,为您的科研保驾护航。
[1] Watanabe H, Yoshida C, Ooishi A, et al. Histidine-Mediated Intramolecular Electrostatic Repulsion for Controlling pH-Dependent Protein-Protein Interaction. ACS Chem Biol. 2019;14(12):2729-2736.
[2] Gahtori P, Gunwant V, Pandey R. How Does pH Affect the Adsorption of Human Serum Protein in the Presence of Hydrophobic and Hydrophilic Nanoparticles at Air-Water and Lipid-Water Interfaces?. Langmuir. 2023;39(44):15487-15498.
[3] Chen H, Ma M, Zhang L, et al. An effective strategy based on electrostatic interaction for the simultaneous sequential purification and isolation of exosomes. Mikrochim Acta. 2025;192(4):259.
*常见问题汇总
Q1:蛋白质纯化过程中主要包含哪些核心分子间作用力?
A:蛋白质纯化的本质是利用目标蛋白与杂蛋白的分子间作用力差异实现差异化分离,核心分子间作用力包含静电相互作用、疏水相互作用、氢键、范德华力及特异性亲和作用力五大类,分别对应主流纯化工艺。
(1)静电相互作用依靠蛋白表面带电氨基酸残基,受缓冲液pH与离子强度调控,是离子交换层析的核心原理,pH偏离蛋白等电点时蛋白带电性增强,可与带电介质可逆结合,适配重组蛋白粗纯化除杂。
(2)疏水相互作用源于蛋白表面疏水氨基酸残基的疏水聚集效应,高盐环境下会显著增强,是疏水作用层析的核心,多用于重组蛋白精细纯化。
(3)氢键与范德华力属于弱分子作用力,贯穿所有层析工艺,主要辅助蛋白与介质结合,同时维系蛋白空间构象。特异性亲和作用力属于精准分子识别作用,依托配体与标签蛋白、抗原抗体的专属结合特性,支撑亲和层析工艺,是重组标签蛋白制备、高纯度蛋白获取的核心技术。各类作用力相互配合,构成了重组蛋白从粗提、精制到抛光的全套纯化体系。
Q2:各类分子间作用力如何影响重组蛋白稳定性与纯化收率?
A:重组蛋白的空间构象稳定性完全依赖分子内氢键、疏水相互作用、静电相互作用维系,而纯化过程中的分子间作用力会直接改变蛋白构象,影响最终收率与产品质量。
首先,分子内疏水相互作用可包裹蛋白内部疏水基团,维持蛋白结构紧凑稳定,若纯化缓冲液盐浓度失衡,会打破疏水平衡,导致蛋白表面疏水基团暴露,引发蛋白聚集、沉淀,大幅降低纯化收率。
其次,静电相互作用决定蛋白溶解性,缓冲液pH接近蛋白等电点时,蛋白净电荷趋近于零,静电排斥力消失,分子间聚集概率大幅提升,造成蛋白失活损耗。
此外,氢键易受温度、缓冲液添加剂影响,氢键断裂会导致蛋白二级结构松散,引发变性。而精准调控亲和作用力、稳定弱分子作用力,可减少蛋白构象损伤。在重组蛋白制备实操中,通过优化缓冲液体系、调控离子强度与pH,平衡各类分子间作用力,能够有效提升蛋白稳定性,将纯化收率最大化。
Q3:疏水相互作用为何是重组蛋白纯化中最关键的非特异性作用力?
A:在重组蛋白制备与纯化流程中,疏水相互作用是影响分离效果、蛋白稳定性与产品纯度的核心非特异性作用力。重组蛋白经原核、真核表达后,表面会暴露大量疏水氨基酸残基,而水溶液极性较强,会驱动蛋白疏水基团相互聚集,这既是蛋白易发生聚集沉淀的核心原因,也是疏水层析分离蛋白的关键依据。
相较于静电作用易受pH、盐离子干扰,氢键作用力较弱且稳定性差,疏水相互作用适配绝大多数可溶性重组蛋白的纯化场景,适用范围更广。在实操中,通过高盐缓冲液压缩水分子层,可强化蛋白与疏水介质的结合,再通过梯度降低盐浓度,减弱疏水作用力,实现目标蛋白与杂蛋白的分步洗脱。同时,疏水相互作用条件温和,不会破坏蛋白二级、三级结构,能够最大程度保留重组蛋白生物活性,规避纯化过程中蛋白变性失活、稳定性下降的问题,因此成为重组蛋白精细纯化、活性蛋白制备的核心作用力。
Q4:静电相互作用在离子交换层析中如何调控重组蛋白分离效果?
A:静电相互作用是离子交换层析的核心原理,也是重组蛋白粗纯化阶段最核心的分子作用力,其强弱直接决定蛋白结合、洗脱效率与分离纯度。蛋白质表面的酸性、碱性氨基酸残基可随缓冲液pH改变带电状态,当缓冲液pH低于蛋白等电点,蛋白带正电,可结合阳离子交换介质;pH高于等电点则带负电,适配阴离子交换介质,依靠静电吸附实现蛋白固定。
纯化过程中,静电相互作用强度受离子强度精准调控,低离子强度缓冲液可消除游离离子干扰,强化蛋白与层析介质的静电结合能力,最大化吸附目标蛋白;逐步提升盐浓度时,缓冲液中游离离子会竞争介质结合位点,打破静电相互作用,实现梯度洗脱。不同蛋白的带电残基数量、分布存在差异,静电结合强度各不相同,因此可通过精准调控pH与盐浓度,区分目标重组蛋白与杂蛋白,高效去除核酸、杂蛋白等杂质,完成重组蛋白前期粗纯化,为后续精细纯化奠定基础。
Q5:重组蛋白制备中如何调控分子作用力减少蛋白聚集与变性?
A:重组蛋白表达与纯化全程可通过针对性调控各类分子间作用力,规避蛋白聚集、变性、失活等问题,提升蛋白稳定性与成品质量。
首先针对疏水相互作用,纯化体系需避免过高盐浓度,同时添加甘油、海藻糖等稳定剂,弱化蛋白表面疏水基团的相互聚集效应,防止蛋白疏水聚集沉淀。
其次调控静电相互作用,规避缓冲液pH接近蛋白等电点,通过微调pH增大蛋白分子净电荷,强化分子间静电排斥力,抑制蛋白聚集。同时优化缓冲液离子强度,避免高盐破坏蛋白分子内氢键与空间构象。
除此之外,全程控制低温环境,减少热运动对氢键、范德华力等弱分子作用力的破坏,稳固蛋白三维结构。针对亲和纯化体系,需控制缓冲液酸碱度温和,避免极端环境破坏特异性亲和作用力,同时防止蛋白构象解体。通过多维度平衡疏水、静电、氢键等核心作用力,可有效解决重组蛋白制备过程中常见的稳定性差、聚集损耗、变性失活等痛点。
-
 400-621-6806
400-621-6806 -
 3599163699
3599163699 -
 周一至周五 9:00-18:00
周一至周五 9:00-18:00 -

-
 0
0
-





